[2012·东北哈师大附中、东北师大附中、辽宁省实验中学第二次联合模拟]某同学为了探究铜与浓硫酸的反应,进行了如下实验。
【实验1】铜与浓硫酸反应,实验装置如图所示。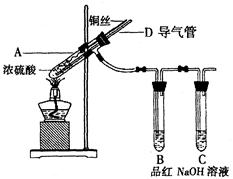
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将铜丝向上提至离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是 。
(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操是 。
【实验2】实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:
①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。
②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如下图的实验: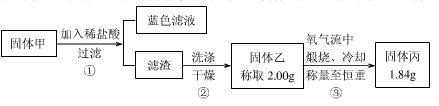
(4)②中检验滤渣是否洗涤干净的实验方法是 。
(5)③中在煅烧过程中一定发生的反应的化学方程式为 。
(6)下列对于固体甲的成分的判断中,正确的是(填字母选项) 。
| A.固体甲中,CuS和Cu2S不能同时存在 |
| B.固体甲中,CuO和Cu2O至少有一种 |
| C.固体甲中若没有Cu2O,则一定有Cu2S |
| D.固体甲中可能有Cu2S |
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如右图所示的装置图:
]请回答下列问题:
(1)写出Al和NaOH溶液反应的离子方程式_______________________________。
(2)在点燃H2之前必须先进行____________________________________________。
(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危险的原因是___________________________。
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进。在改进后的实验中H2的生成速率______________________。(填“减慢”或“加快”)
(5)2.3 g钠投入20 mL水中完全反应放出的气体在标准状况下的体积是_____________,所得溶液的物质的量浓度是______________________。(不计溶液体积的变化)
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图8-9所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
图8-9
(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为 。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为 ;装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是 。一段时间后,C中白色沉淀溶解,其原因是 。
(3)装置D的作用是 。
某研究性学习小组为完成浓硝酸、稀硝酸、NO2、NO的部分实验,并有效地防止NO2、NO的污染。设计了如下图所示的装置进行实验。
先将适量块状CaCO3和过量铜片放入底部开一小孔的试管中,塞上塞子(连有带活塞的导气管),如图A所示,再将试管放入盛有适量盐酸的烧杯中,打开活塞,发生反应:CaCO3+2HCl====CaCl2+H2O+CO2↑,用产生的CO2排尽试管内的空气。
(1)待CaCO3反应完全后,关闭活塞,在导气管上套一排尽空气的气球,然后将试管放入盛有浓硝酸的大试管中,如图B所示。再打开活塞,观察到的现象是_________________。上述现象说明____________________________________________________。有关反应的离子方程式为_____________________________________________________________________。
(2)上述反应进行一段时间后,关闭活塞,迅速将带小孔的试管取出,放入盛有适量水的烧杯中,如图C所示,再打开活塞,观察到的现象是_______________________________。
(3)关闭活塞,迅速将试管取出,放入盛有足量NaOH溶液的烧杯中,如图D所示。打开活塞,NO、NO2与NaOH溶液发生反应:2NaOH+NO+NO2====2NaNO2+H2O,气球逐渐变小,试管内液面上升。NO不能单独与NaOH溶液反应,若要将氮的氧化物完全吸收,应该如何操作?___________________________________________________。
如图所示装置是某种气体X的发生装置和收集装置(必要时可加热)。所用的试剂从下列试剂中选取2—3种;硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水。
请完成下列问题:
(1)气体X的化学式是____________。
(2)所选药品a是____________,b是____________,装置B的作用是____________。
(3)用所选的药品发生反应生成X时,离子方程式是___________________________。
(4)反应刚开始时A中的主要现象是____________。
下图是铜与稀硝酸反应的两个实验装置图,请完成下列问题:
(1)铜与稀硝酸反应的离子方程式:____________________________________________。
(2)Ⅰ实验装置中能否证明铜与稀硝酸反应生成的是NO气体____________(填“能”或“不能”),简述理由_______________________________________________________________。
(3)若用Ⅱ实验装置进行实验,证明铜与稀硝酸反应生成的气体是NO,则:检查装置气密性的操作是________________________;在烧杯中加入一定体积的稀硝酸,打开止水夹,用注射器慢慢抽取干燥管内的空气,稀硝酸沿着干燥管慢慢上升,直到充满整个干燥管,停止抽拉注射器,关闭止水夹,观察干燥管内的现象_______________________;反应停止后,打开止水夹,用注射器抽取干燥管内的气体(事先已将注射器内原有的空气推出),关闭止水夹后取下注射器,并抽取一定量的空气,观察到的现象是_____________________________。
(4)上述实验完成后,将注射器内的气体通入到NaOH溶液中,其目的是_________________。