短周期主族元素X、Y、Z、W,原子序数依次增大。X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半。下列叙述正确的是
A.非金属性: |
B.原子半径: |
C.最高价氧化物对应水化物的酸性: |
| D.单质Y常温下能溶于浓硝酸 |
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是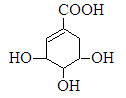
| A.分子式为C7H6O5 |
| B.分子中含有2种官能团 |
| C.可发生加成和取代反应 |
| D.在水溶液羧基和羟基均能电离出H+ |
下列说法正确的是
A.按系统命名法,化合物 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 |
| B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 |
| C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
D.结构片段 的高聚物,其单体是苯酚和甲醛 的高聚物,其单体是苯酚和甲醛 |
氰酸铵(NH4OCN)与尿素[CO(NH2)2]
| A.都是共价化合物 | B.都是离子化合物 |
| C.互为同分异构体 | D.互为同素异形体 |
下列关于实验室制备乙酸乙酯和乙酸丁酯的描述正确的是
| A.均采用水浴加热 | B.制备乙酸丁酯时正丁醇过量 |
| C.均采用边反应边蒸馏的方法 | D.制备乙酸乙酯时乙醇过量 |
根据有机化合物的命名原则,下列命名正确的是
A. 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 |
B.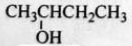 2-羟基丁烷 2-羟基丁烷 |
| C.CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
| D.CH3CH(NH2)CH2COOH 3-氨基丁酸 |