现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为_________热反应,且m+n ________ p(填“>”、“=”或“<”)。
(2)减压时,A的质量分数________(填“增大”、“减小”或“不变”,下同)。
(3)若容积不变加入B,则A的转化率__________,B的转化率________。
(4)若升高温度,则平衡常数k将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色________;而维持容器内压强不变,充入氖气时,混合物颜色___________(填“变深”、“变浅”或“不变”)。
将10mol A和5mol B放入10L真空箱内,某温度下发生反应:3A(气)+B(气) 2C(气)在最初0.2s内,消耗A的平均速率为0.06mol·(L·S)-1.则在0.2s时,真空箱中C的物质的量是
2C(气)在最初0.2s内,消耗A的平均速率为0.06mol·(L·S)-1.则在0.2s时,真空箱中C的物质的量是
| A.0.12mol | B.0.08mol | C.0.04mol | D.0.8mol |
下列说法正确的是
| A.SO2和SO3互为同分异构体 |
| B.液溴和溴蒸气是同素异形体 |
| C.金刚石和石墨都是由碳原子构成,因此它们是同种物质 |
| D.乙醇和二甲醚互为同分异构体 |
下列各选项中两种粒子所含电子数不相等的是
| A.羟基(-OH)和氢氧根(OH-) | B.甲烷(CH4)和铵根(NH4+) |
| C.氨气(NH3)和水(H2O) | D.双氧水(H2O2)氯化氢(HCl) |
环境与可持续发展是现在国际的主题,利用海水是可持续发展的一个任务,对于海水的利用认识错误的是
| A.海水中有大量人类需要的物质,人类可以大量开发海水中的物质,以满足资源短缺的问题。 |
| B.海水可以成为廉价的能源基地,但不能开发过度,要适度使用和开发 |
| C.可以用太阳能电解海水以获取氢能源 |
| D.人类在利用海水时要兼顾海洋生物和海洋生态平衡 |
现有乙酸、乙烯和丙烯(C3H6)的混合物,其中氧的质量分数为a,则碳的质量分数是()
A. |
B.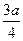 |
C. |
D.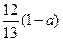 |