已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+。下列叙述不正确的是( )
| A.氧化产物为Cl2 |
| B.氧化剂与还原剂的物质的量之比为1∶2 |
| C.若有3mol H2O生成,则反应中有2mol电子转移 |
| D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移 |
根据如图,可判断出下列离子方程式中错误的是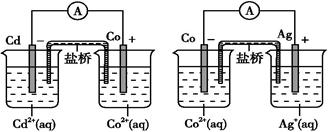
A.2Ag(s)+Cd2+(aq) 2Ag+(aq)+Cd(s) 2Ag+(aq)+Cd(s) |
B.Co2+(aq)+Cd(s) Co(s)+Cd2+(aq) Co(s)+Cd2+(aq) |
C.2Ag+(aq)+Cd(s) 2Ag(s)+Cd2+(aq) 2Ag(s)+Cd2+(aq) |
D.2Ag+(aq)+Co(s) 2Ag(s)+Co2+(aq) 2Ag(s)+Co2+(aq) |
用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内物质),能使溶液恢复到原来的成分和浓度的是
| A.AgNO3[AgNO3] | B.NaOH[NaOH] |
| C.KCl[KCl] | D.CuSO4[CuO] |
如下图所示,各容器中盛有海水,铁在其中被腐蚀时,由快到慢的顺序是
| A.4>2>1>3 | B.2>1>3>4 |
| C.4>2>3>1 | D.3>2>4>1 |
下列物质一定属于同系物的是
| A.④和⑧ | B.④和⑥ | C.⑤和⑧ | D.①和② |
主链含5个碳原子,有甲基、乙基2个支链的烷烃有
| A.2种 | B.3种 | C.4种 | D.5种 |