下列图示与对应的叙述相符的是( )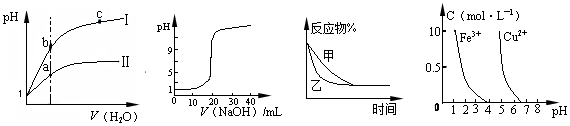
图1 图2 图3 图4
| A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2表示0.1000 mol·L-1CH3COOH溶液滴定20.00mL0.1000 mol·L-1NaOH溶液所得到的滴定曲线 |
C.图3表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
下列各组物质性质的比较正确的是
| A.酸性:H3PO4>H4SiO4>H2CO3 | B.熔沸点:H2O> H2Se > H2S |
| C.离子半径:S2->Cl->K+ | D.离子的氧化性:Na+>Mg2+>Al3+ |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
L |
M |
X |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
﹢2 |
﹢3 |
﹢6、﹣2 |
﹢2 |
﹣2 |
下列叙述正确的是()
| A.离子半径大小:r(M3﹢)>r(T2﹣) | B.R的氧化物对应的水化物可能具有两性 |
| C.X单质可在氧气中燃烧生成XO3 | D.L、X形成的简单离子核外电子数相等 |
0℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g)  2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是:
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是:
①N2O4的消耗速率与NO2的生成速率之比为1:2②NO2的生成速率与NO2消耗速率相等③烧瓶内气体的压强不再变化④烧瓶内气体的质量不再变化⑤NO2的物质的量浓度不再改变⑥烧瓶内气体的颜色不再加深⑦烧瓶内气体的平均相对分子质量不再变化⑧烧瓶内气体的密度不再变化。
| A.②③⑥⑦ | B.①④⑧ | C.只有①④ | D.只有⑦⑧ |
下列反应的离子方程式正确的是:
| A.次氯酸钙溶液中通入过量二氧化碳 Ca2+ + 2ClO- + H2O + CO2 ="=" CaCO3¯ + 2HClO |
| B.硫酸亚铁溶液中加过氧化氢溶液 2Fe2+ + H2O2 + 2H+ ==2Fe3+ + 2H2O |
| C.用氨水吸收少量二氧化硫 NH3·H2O + SO2 ="=" NH  + HSO + HSO |
| D.硝酸铁溶液中加过量氨水 |
Fe3+ + 3NH3·H2O ="=" Fe(OH)3¯ + 3NH
将足量BaCO3粉末分别加入下列溶液中,充分溶解至溶液饱和。各溶液中Ba2+的浓度最小的为:
| A.40mL 水 | B.10mL 0.2mol/LNa2CO3溶液 |
| C.50mL 0.01mol/L 氯化钡溶液 | D.100mL 0.01mol/L盐酸 |