已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下: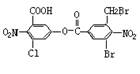
1mol该有机物与足量的氢氧化钠溶液混合并加热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑醇羟基和硝基与氢氧化钠的反应,下同),溶液蒸干得到的固体产物产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为b,则a、b分别是( )
| A.5mol、10mol | B.6mol、2 mol |
| C.8mol、2 mol | D.8mol、4mol |
最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如下图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解。一般认为,放电时,电池中的反应如下: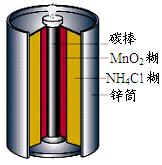
E极:2MnO2+2H2O+2e-="==" 2MnO(OH)+2OH-
F极:Zn+2NH4Cl -2e-===Zn(NH3)2Cl2+2H+
总反应式:2MnO2+Zn+2NH4Cl ="==" 2MnO(OH)+Zn(NH3)2Cl2
下列说法正确的是
| A.E极是电池的正极,发生的是氧化反应 |
| B.F极是电池的负极,发生的是氧化反应 |
| C.从结构上分析,锌锰电池应属于可充电电池 |
| D.锌锰电池内部发生的氧化还原反应是可逆的 |
下列烧杯中盛放的都是稀硫酸,不能构成原电池的是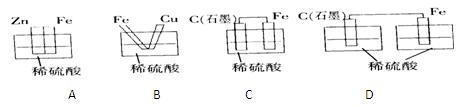
将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程中正确的是
| A.1/2 N2H4(g)+ 1/2 O2(g)= 1/2 N2(g)+ H2O(l)△H=+257kJ·mol-1 |
B.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-133.5kJ·mol-1 |
C.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=+534kJ·mol-1 |
D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ·mol-1 |
下列说法正确的是
| A.酸性氧化物在常温下均呈气态 |
| B.元素的非金属性越强,对应离子的还原性也越强 |
| C.非金属元素间相互结合形成的化合物一定是共价化合物 |
| D.共价化合物的分子中一定不含离子键 |