工业上目前使用两种方法制取乙醛:(1)乙炔水化法;(2)乙烯氧化法。下列两表提供生产过程中原料、反应条件、原料平衡转化率、产量等有关的信息情况:
表一:原料、反应条件、平衡转化率、日产量
| |
乙炔水化法 |
乙烯氧化法 |
| 原料 |
乙炔、水 |
乙烯、空气 |
| 反应条件 |
HgSO4、100~125℃ |
PdCl2-CuCl2、100~125℃ |
| 平衡转化率 |
乙炔平衡转化率90%左右 |
乙烯平衡转化率80%左右 |
| 日产量 |
2.5吨(某设备条件下) |
3.6吨(相同设备条件下) |
表二:原料来源生产工艺
| |
原料生产工艺过程 |
| 乙炔 |
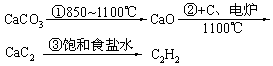 |
| 乙烯 |
来源于石油裂解气 |
根据上述两表,回答下列问题:
(1)写出下列化学方程式:
a.乙炔水化法制乙醛__________________________________________________。
b.乙烯氧化法制乙醛______________________________________________。
(2)从两表中分析,现代工业上乙烯氧化法逐步取代乙炔水化法(从环境、原料来源、产率和产量、能耗等角度),分析可能的原因:________________________________。
(3)从化学反应速率角度分析,在相同条件下,两种制取乙醛的方法哪种快?
___________________________________________________________________。
(4)若将上述两种方法的反应条件,均增加“100atm”,原料平衡转化率_______(填增大、减小、不变);而实际生产中不采用的理由是_____________________________。
(5)若乙烯由石油裂化(裂化气混合气体的平均化学式CnHm、m>2n),进一步完全催化裂解而来,得到体积百分含量分别为:甲烷:5%、乙烯:40%、丙烯:10%、其余为丁二烯和氢气(气体体积均在同温同压下测定)。若得到40mol乙烯,求:能够得到丁二烯和氢气的物质的量各为多少?
(15分)合成氨工厂常通过测定反应前后混合气体的密度来确定氮的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.553 6 g·L-1(标准状况),从合成塔中出来的混合气体在相同条件下的密度为0.693 g·L-1 (标准状况)。求该合成氨厂N2的转化率。
某化工厂每小时生产98%(质量分数)硫酸a t(吨),为使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求燃烧后的混合气体中含氧气的体积分数为b%。若空气中氧气的体积分数为21%,且不考虑各生产阶段的物料损失,求:
(1)该厂每小时消耗标准状况下空气的体积。
(2)为满足题设需求,b%的下限。
在给定温度下发生下述反应:4FeS2(s)+11O2(g)====2Fe2O3(s)+8SO2(g) ΔH="-3" 319 kJ/mol,又知反应后的固体残渣中含有4%的FeS2,试计算燃烧1kg这种硫铁矿时放出的热量。
1 mol某直链烷烃A,可以直接裂解成1mol气态烷烃B和1mol气态烯烃C。已知此裂解气的平均相对分子质量与空气的平均相对分子质量相同。请完成下列问题:
(1)A可能是____________;C可能是____________。
(2)若将1体积B完全燃烧,需2体积O2(气体体积在同温同压下测定),则C应是____________。该烯烃发生加聚反应的化学方程式为___________________________。
地球上海水资源丰富,但淡水资源紧缺。据专家们估计,地球表面积的71%是海洋,地球上淡水只占总水量的2.5%,而淡水中很大一部分又被南极洲、格陵兰和北极的冰山或冰川以冰的形式封存起来,剩下来的大部分为地下水。所有的湖泊、溪流、江河和雨水则仅占淡水总量的0.1%还不到。
(1)已知海洋的平均深度为3.8 km,地球的平均半径为6 371 km,海水的平均密度为1.03×103 kg/m3。你能估算地球上海水的总体积和海水的总质量吗?(用3位有效数字表示)
(2)你能估算地球上所有的湖泊、溪流、江河中淡水总质量吗?(用3位有效数字表示)
(3)地球上海水资源丰富,但淡水资源紧缺。你知道可用哪些物理方法淡化海水吗?