已知:
⑴H2(g) + 0.5O2(g) =H2O(g) △H1=a kJ/mol
⑵2H2(g) + O2(g) = 2H2O(g) △H2=b kJ/mol
⑶H2(g) + 0.5O2(g) =H2O(l) △H3=c kJ/mol
⑷2H2(g) + O2(g) = 2H2O(l) △H4=d kJ/mol
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
下列有关说法正确的是
| A.25℃101kPa时,CH4(g)+2O2(g)=CO2(g) +2H2O(g)△H=-Q kJ/mol,则甲烷的燃烧热为Q kJ/mol |
| B.CaCO3(s)=CaO(s)+CO2(g) 室温下不能自发进行,说明该反应的 ΔH<0 |
C.反应N2(g)+3H2(g) 2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大 2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大 |
| D.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2的值均大于零):H2(g) +Cl2(g)=2HCl(g),△H1=—Q1 kJ/mol,H2(g) +Br2(g)=2HBr(g),△H2=—Q2 kJ/mol,则△H1<△H2 |
关于反应3A (g)+ B (g)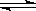 2 C (g) 发生过程中的能量变化如图,下列说法中不正确的是
2 C (g) 发生过程中的能量变化如图,下列说法中不正确的是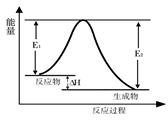
| A.该反应为放热反应 |
| B.反应体系中加入催化剂, E1、E2减小,△H不变 |
| C.增大反应体系压强,化学平衡正向移动,气体B的浓度减少 |
| D.降低反应体系温度,反应速率减慢,A的转化率增大 |
下图是可逆反应A+2B 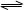 2C+3D的化学反应速率与化学平衡随外界条件改变(降温和加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(降温和加压)而变化的情况,由此可推断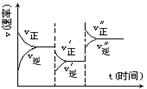
A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应
D.A、B、C、D均为气体
已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径A>B>D>C | B.原子序数d>c>b>a |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
下列说法正确的是
①水分子之间存在氢键,所以水受热不易分解
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔化状态下能导电的物质不一定是离子化合物
⑦有单质生成的反应一定是氧化还原反应
⑧碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
| A.③⑤⑥⑦⑧ | B.②③④⑥⑦ |
| C.③⑥⑧ | D.①③④⑥ |