用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是C
| A.3∶2∶2 | B.1∶2∶3 | C.1∶3∶3 | D.3∶1∶1 |
根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱,按照这个理论,下列微粒中既属于酸又属于碱的物质是()
①HS- ②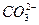 ③
③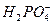 ④NH3 ⑤H2S ⑥CH3COOH ⑦OH- ⑧H2O
④NH3 ⑤H2S ⑥CH3COOH ⑦OH- ⑧H2O
| A.①② | B.①③⑧ | C.①⑤ | D.③⑥ |
下列物质都不能使酸性高锰酸钾溶液褪色的是()
| A.乙烯和1,3-丁二烯 |
| B.甲烷和正丁烷 |
| C.苯和甲苯 |
| D.乙炔和乙醛 |
在一定条件下,在密闭容器中进行的反应aX(g)+bY(g) cZ(g)+dW(g),5 min后达到平衡,X减少n mol·L-1,Y减少
cZ(g)+dW(g),5 min后达到平衡,X减少n mol·L-1,Y减少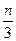 mol·L-1,Z增加
mol·L-1,Z增加 mol·L-1。在其他条件不变时,将容器体积增大,W的百分含量不发生变化。则化学方程式中各物质的化学计量数之比a∶b∶c∶d应为()
mol·L-1。在其他条件不变时,将容器体积增大,W的百分含量不发生变化。则化学方程式中各物质的化学计量数之比a∶b∶c∶d应为()
| A.1∶3∶1∶2 | B.3∶1∶2∶2 | C.3∶1∶2∶1 | D.1∶3∶2∶2 |
反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是()
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是()
| A.容器内压强不再变化 |
| B.Fe3O4的物质的量不变 |
| C.v(H2O)=v(H2) |
| D.反应不再进行 |
在如下图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是()
| A.碳棒上有气体放出,pH变大 |
| B.a是正极,b是负极 |
| C.导线中有电子流动,电子从a极到b极 |
| D.a极上发生了氧化反应 |