课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3、还含有少量NaCl,其它杂质不计)和石灰乳(氢氧化钙的悬浊液)为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
【粗产品成分分析】
(1)取适量粗产品溶于水,加入Ba(NO3)2溶液出现白色浑浊,该反应的化学方程式为 ,由此该粗产品中一定不含有 。
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
【含量测定】Na2CO3含量的测定
(1)该兴趣小组的同学设计了下图所示的实验装置。取20.0g粗产品,进行实验。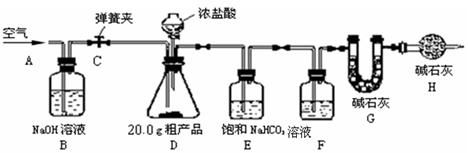
【说明】①碱石灰是CaO与NaOH的固体混合物。
②CO2在饱和NaHCO3溶液中的溶解度非常小。
(2)操作步骤:
①连接好装置,检查气密性;将药品加入各装置
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量G的质量;
④关闭弹簧夹C,慢慢滴加浓盐酸,直至D中无气泡冒出;
⑤打开弹簧夹C,再次缓缓通入一段时间空气;
⑥再次称量G的质量,得前后两次质量差为0.48g。
(3)问题探究:
①在用托盘天平称量粗产品时,如果天平的指针向右偏转,说明 。
②B装置的作用是 。
③在步骤②中,A处缓缓通入一段时间空气的目的是 。
④若没有H装置,则测定的Na2CO3的质量分数会 (填“偏大”、“偏小”、“不变”)。
⑤该兴趣小组指导老师认为该方案有些不合理,指导同学们更换了其中的一种试剂并去掉了一个装置后实验得到了完善,并测得20.0 g粗产品只能产生0.44 g CO2。你认为更换后的试剂是 ,原实验中实验值0.48g比正确值0.44 g偏大的原因是(假设操作均正确) 。(4)数据计算:
根据正确值0.44 g,求得粗产品中Na2CO3的质量分数是 (写出计算过程)。
6月26日是"国际禁毒日"。毒品严重危害人的身心健康和生命安全,吸食毒品后会使人产生强烈的兴奋和致幻效果,作用快,易成瘾。我们要加深对毒品危害的认识,远离毒品。"冰毒"是毒性极强的毒品之一,化学式为
,请计算:
(1)一个冰毒(
)分子中含有个原子;
(2)冰毒中碳、氢、氮元素的质量比是;
(3)冰毒中氢元素的质量分数是(计算结果精确到0.1%)。
6.5g锌与200g稀硫酸恰好完全反应,求:
(1)可制得氢气多少克?
(2)稀硫酸中溶质的质量分数是多少?
某炼铁厂若要练出1120t含碳5%的生铁,需要含氧化铁80%的赤铁矿多少吨?
无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。某品种茄子的无土栽培营养液中含有6%的KNO3。
(1)KNO3属于___________(填“钾肥”“氮肥”或“复合肥料”);
(2)KNO3的相对分子质量为______;
(3)KNO3中钾、氮、氧元素的质量比为______________;
(4)要配制150 kg该营养液,需要KNO3的质量为多少千克?_______
下图是病人输液时用的一瓶葡萄糖注射液标签,请根据标签给出的数据计算该溶液中含水g,溶液的密度约为g/cm3。