某课外活动小组同学用图一装置进行实验,试回答下列问题。
(1)① 若开始时开关K与a连接,则铁发生的是电化学腐蚀中的 腐蚀;
② 若开始时开关K与b连接,则总反应的离子方程式 。
(2)芒硝(化学式为Na2SO4·10H2O),无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法。用如图二所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是提高原料的利用率来看都更加符合绿色化学理念。
① 该电解槽的阳极反应式为: ,此时通过阴离子交换膜的离子数 (填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
② 制得的氢氧化钠溶液从出口(选填“A”、“B”、“C”、“D”) 导出。
③ 若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为 。已知H2的燃烧热为285.8 kJ/mol,则该燃料电池工作产生36 g H2O时,理论上有 kJ的能量转化为电能。
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为;
(2)反应开始至5min Z的平均反应速率为, X的转化率为;
(3)5min后Z的生成速率比5min末Z的生成速率大、小、相等)。
处于相邻2个周期的主族元素A、B、C、D。它们原子半径依次减小。A离子和B离子的电子层相差2层,且能形成BA2型的离子化合物。C的离子带3个单位正电荷。D的气态氢化物通式为H2R,在其最高价氧化物中D质量分数为40%。D的原子序数大致等于其原子量数值的一半。试回答
①A是______ B是______ C是______ D是______(填元素符号)
②B、C、D单质的还原性从大到小的顺序是___________。
③向D的氢化物的水溶液中,滴入少量A单质的水溶液,写出反应方程式_____________________________________。
下表是周期表中的一部分,根据元素A—I在周期表中的位置,用元素符号或化学式回答下列问题:
 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
|||||||
| 2 |
D |
E |
G |
I |
||||
| 3 |
Bm] |
C |
F |
H |
(1)表中元素,化学性质最不活泼的是,氧化性最强的单质是, (2)最高价氧化物的水化物碱性最强的是,酸性最强的是;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的是;
(4)在B、C、D、E、F、G、H中,原子半径最大的是.
离子半径最大的是.写出AEH形成的一种盐(化肥)的电子式.
.有机化学反应因反应条件不同,可生成不同的有机产品。例如:
(一)苯的同系物与卤素单质混合,在光照条件下,侧链上的氢原子被卤素原子取代;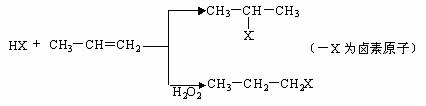
(二)工业上利用上述信息,按下列路线合成结构简式为的物质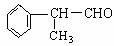 ,该物质是氢化阿托醛一种香料。
,该物质是氢化阿托醛一种香料。
请根据上述路线,回答下列问题:
(1)A为一氯代物,它的结构简式可能为_______________________________________。
(2)工业生产过程中,中间产物必须经过②③④得到D,而不采取直接转化为D的方法原因是_____________________________________。
(3)写出反应类型②_________、③_________。
(4)反应④的化学方程式为:__________________________________________。
(5)氢化阿托醛与氢气1:1加成后的产物C9H10O的同分异构体很多,写出两种符合下列三个条件的 C9H10O的同分异构体的结构简式:__________________、___________________。
①能与溴水反应
②能与氢氧化钠溶液反应
③分子中只有苯环一种环状结构,苯环上有两个取代基,且苯环上的一溴代物有两种;
(6)氢化阿托醛发生银镜反应的化学方程式为_____________________________________。
(12分)据《中国制药》报道,化合物F是用于制备“非典”药品(盐酸祛炎痛)的中间产物,其合成路线为:
已知:(Ⅰ)RNH2+R/CH2Cl  RNHCH2 R/+HCl(R和R/代表烃基)
RNHCH2 R/+HCl(R和R/代表烃基)
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
(Ⅲ)
(苯胺,弱碱性,易氧化)
(Ⅳ) 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
回答下列问题:
(1)反应①的条件是_______________________________
(2)反应③和反应④的顺序不能颠倒,原因是_____________________________________
(3)C的结构简式是_________________。
(4)D+E→F的化学方程式:_____________________。
(5)反应①~⑤中,属于取代反应的是(填反应序号)_______________ 。