如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2 A(?)+B(?) x C(g);ΔH<0
x C(g);ΔH<0
平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。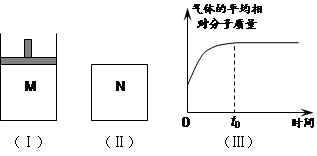
⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
| 可能的情形 |
A、B是否为气态 |
z与y的大小关系 |
M(B)与M(C)的大小关系 (M表示摩尔质量) |
|
| A |
B |
|||
| ① |
是 |
不是 |
z =y |
不确定 |
| ② |
|
|
|
|
| ③ |
|
|
|
|
化学反应的限度是当___和__相等,反应物和生成物的__保持不变时,所达到的一种看似的“平衡状态”。
用电子式表示:
CaCl2的形成过程______NaOH的电子式___ Cl2 的电子 式___
式___
下列反应中,属于放热反应的是。
① 煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ② 燃烧木炭取暖③生石灰与水反应 ④ 酸与碱的中和反应⑤ 氢气还原氧化铜 ⑥ 炽热的铁粉与水蒸气的反应
原电池是把转化成___的装置,其反应的实质是_。
写出铜锌原电池(稀硫酸为介质)的电极反应:
正极,负极。
在第3周期中,化学性质最稳定的元素符号是,最高价氧化物的水化物的酸性最强的化合物的化学式是,碱性最强的化合物的化学式是,显两性的氢氧化物的化学式是,该两性氢氧化物与氢氧化钠溶液反应的离子方程式为。