实验室可通过多条途径得到氮气,常见的三种方法是:
方法一:将氨气通过灼热的氧化铜粉末,得到纯净的氮气和铜。
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末。
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,逸出氮气。
下列是进行实验时可选择的实验仪器(其它必要的仪器如:铁架台、铁夹、铁圈、石棉网、
酒精灯等未列出):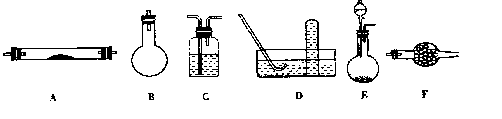
请回答下列问题:
(1)方法一制氮气:氨气是用浓氨水跟生石灰反应得到,此反应最好选用(填仪器的编号)
_________作发生装置,该反应的化学方程式_________________________。
要制取并收集纯净的氮气(可含有少量的水),还应使用上述仪器中的(填仪器的编号,
并按气流方向从左向右列出)_______________________________________________。
(2)制取氮气的三种方法中,方法一和方法二越来越受到人们的关注,经常被联合使用。
这两种方法与方法三相比,其优越性在于①____________ ______________________,
②_________________________________________。(至少写两点)
(8分)实验室里用加热正丁醇、溴化钠和浓硫酸的混合物的方法来制备1-溴丁烷时,还会有烯、醚和溴等副产物生成,反应结束后将反应混合物蒸馏,分离得到1-溴丁烷。已知有机物具有如下性质:
| 熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
|
| 正丁醇 |
-89.53 |
117.25 |
0.81 |
| 1-溴丁烷 |
-112.4 |
101.6 |
1.28 |
| 丁醚 |
95.3 |
142 |
0.76 |
| 1-丁烯 |
-185.3 |
-6.5 |
0.59 |
试完成下列问题:
(1)生成1溴丁烷的反应的化学方程式是______________________________________。
(2)反应中由于副反应而生成副产物的反应类型是______________________________。
(3)反应加热的温度应__________100 ℃(填“大于”“小于”或“等于”)
(4)反应结束时,从反应混合物中蒸馏得到1-溴丁烷时,应控制的温度范围是____________;选用的装置应是图中的__________ (填序号)。
(5)蒸馏得到的馏分中可能含有的杂质主要是__________,将其进一步除去的方法是________________________________________。
(10分)实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取W g该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按图所示装置进行实验。
请完成下列有关问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是______________________。
(2)装置图中需要加热的仪器有__________:(用字母填空,下同),操作时应先点燃__________处的酒精灯。
(3)A装置中发生反应的化学方程式是______________________________________。
(4)D装置的作用是______________________________________________________。
(5)读取N2的体积时,应注意:①___________;②___________。
(6)实验中测得N2的体积为V mL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据有___________ (用字母填空)。
| A.生成二氧化碳气体的质量 |
| B.生成水的质量 |
| C.通入氧气的体积 |
| D.氨基酸的相对分子质量 |
某溶液中含有 、
、 、OH-、Cl-,若只允许取两次该溶液而把四种离子分别检验出来,则检验的步骤顺序应为:
、OH-、Cl-,若只允许取两次该溶液而把四种离子分别检验出来,则检验的步骤顺序应为:
(1)先检验________,加入________试剂(或溶液)
(2)然后检验________,加入________试剂(或溶液)。离子方程式为__________________。
(3)再检验________,加入________试剂(或溶液)。离子方程式__________________。
(4)最后检验________,加入________试剂(或溶液)。离子方程式__________________。
某物质可能含有炭粉、CaCO3、CuO、Fe2O3中的一种或几种。现进行如下实验:
(1)取样品,加热至高温,产生一种能使澄清石灰水变浑浊的无色气体。
(2)往冷却后的固体残渣中加入足量的稀HCl,固体残渣全部溶解,同时产生一种可燃气体。
根据上述实验推断:该物质中一定含有________,一定不含有________,可能含有________。写出有关反应的化学方程式,属于氧化还原反应的,标出电子转移的方向和数目。属于离子反应的,写出离子方程式。
用50 mL 0.50 mol · L-1的盐酸与50 mL 0.55 mol · Lf-1的氢氧化钠溶液在如下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。完成下列问题:
(1)烧杯间填满碎泡沫塑料的作用是__________________;
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?______(填“能”或“不能”),其原因是___________________________________;
(3)为什么氢氧化钠溶液的浓度要用0.55 mol · L-1?___________________________;
实验中若改用60 mL 0.50 mol · L-1的盐酸与50 mL 0.55 mol · L-1的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”“不相等”),若实验操作均正确,则所求中和热_________(填“相等”“不相等”);
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:_____________________________;
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得的结果偏低,请你分析结果偏低的原因可能是_________(填字母代号)。
a.测量盐酸的温度后,温度计没有用水冲洗干净
b.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
c.做本实验的当天室温较高
d.将50 mL 0.55 mol · L-1的氢氧化钠溶液取成了50 mL 0.55 mol · L-1的氨水
e.在量取盐酸时仰视读数
f.大烧杯的盖板中间小孔太大