(15分)二氧化硫是大气污染物之一,为粗略测定周围环境中二氧化硫的含量,某课外活动小组的甲、乙两位同学分别用相同实验装置和溶液,测定同一时间, 同一地点空气(含SO2、N2、O2气体,其他气体忽略)中SO2的含量。实验装置如右图反应试管中装有碘的淀粉稀溶液A。 SO2和I2发生反应为:S02+I2+2H20=H2SO4+2HI(N2、02不与I2、 淀粉反应),试回答下列问题: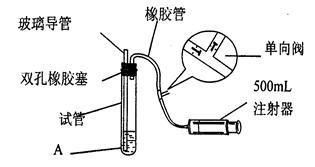
(1)检查该装置气密性时,先在试管中装入适量的水(保证玻璃管的下端浸在水中),然后_____________________(注意阀的单向性),则证明该装置的气密性良好。
(2)若A溶液的体积为VmL,浓度为c mol·L-1,当溶液的颜色刚好变色,停止抽气,此时甲、乙两位同学注射器内抽得气体的体积分别为V甲mL、V乙mL(所有的体积已折算成标况下体积),且V甲>V乙,则甲、乙两个测定结果中与该地点空气中S02的体积分数真实情况最接近的是_______________________(.用含c、V、V甲或V乙…等的关系式表示)。另一位实验结果产生较大误差的原因可能是_______________________________________________
(3)若将上述装置进行改进,除导管外,重新连接装置需要选用的仪器有___________________。 (选下列仪器的编号)
a、烧杯 b、试管 c、锥形瓶 d、容量瓶e、量筒 f、单孔塞 g.双孔塞
(4)欲净化空气,除去空气中的二氧化硫可选用的试剂是___________________。
某化学小组采用类似乙酸乙酯的装置(如下图)用环己醇制备环己烯。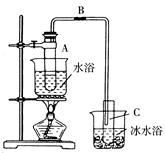
已知:
| 密度(g/cm3) |
熔点(℃) |
沸点(℃) |
溶解性 |
|
| 环己醇 |
0.96 |
25 |
161 |
能溶于水 |
| 环己烯 |
0.81 |
-103 |
83 |
难溶于水 |
(1)制备粗品
将12.5 mL还已醇加入试管A中,再加入1 mL浓硫酸摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是______________,导管B除了导气外还具有的作用是_______________
②试管C置于冰水浴中的目的是__________________
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在__________层(填“上”或“下”),分液后用__________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图装置蒸馏,冷却水从________ 口进入。
蒸馏时要加入生石灰,目的是_______________________
③收集产品时,控制的温度应在__________左右,实验
制得的环己烯精品质量低于理论产量,
可能的原因________(填序号)
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(11分)实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题: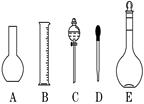
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),
仪器C的名称是,
本实验所需玻璃仪器E规格为 mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
| A.配制一定体积准确浓度的标准溶液 | B.长期贮存溶液 |
| C.用来加热溶解固体溶质 | D.量取一定体积的液体 |
(3)在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线, 则所配制溶液浓度
0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示的3组,第2组中物质X的化学式是 。
| 第1组 |
第2组 |
第3组 |
| S(单质) |
SO2、X、Na2SO3、NaHSO3 |
SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用下图所示的装置研究SO2的性质:
(熔点:SO2-76.1℃,SO3 16.8℃;沸点:SO2-10℃,SO3 45℃)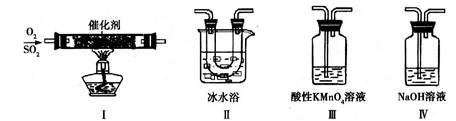
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是 ;
装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是
。
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有70mL 2mol·L-1NaOH溶液,反应后增重5.12g,则装置Ⅳ中发生反应的化学方程式是 。
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。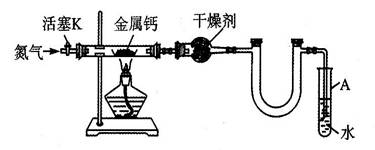
(1)按图连接好实验装置,检查装置的气密性的方法是 。
(2)反应过程中末端导管必须始终插入试管A的水中,目的是 。
(3)制备氮化钙的操作步骤是①打开活塞K并通入N2;②点燃酒精灯,进行反应;
③反应结束后, ;④拆除装置,取出产物。
(4)数据记录如下:
| 直玻管质量m0/g |
直玻管与钙的质量m1/g |
直玻管与产物的质量m2/g |
| 14.80 |
15.08 |
15.15 |
①计算得到实验式CaxN2,其中x= 。
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:
。
用KOH固体配制质量分数为28%的KOH溶液(ρ=1.1g/mL)。
(1)溶液中OH-与H2O分子个数之比为 ,溶液的物质的量浓度为 。
(2)若需配制上述溶液95mL,则需称量KOH固体 克,需用到的玻璃仪器有: 。
(3)容量瓶使用前检漏的操作为: 。
(4)下列操作中,使所得KOH溶液浓度偏大的是 。
| A.称量KOH固体时,直接用纸称量; |
| B.KOH固体溶解后,未完全冷却就转移至容量瓶中; |
| C.定容时,俯视容量瓶标线; |
| D.配制溶液前,容量瓶未完全干燥; |
E、转移溶液时,有少量液体溅出