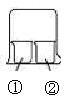
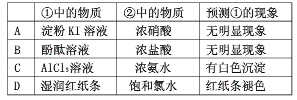
用如下图所示装置进行下列实验,实验结果与预测的现象不一致的是
| |
①中的物质 |
②中的物质 |
预测①的现象 |
| A |
淀粉KI溶液 |
浓硝酸 |
无明显现象 |
| B |
酚酞溶液 |
浓盐酸 |
无明显现象 |
| C |
AlCl3溶液 |
浓氨水 |
有白色沉淀 |
| D |
湿润红纸条 |
饱和氯水 |
红纸条褪色 |
下列叙述正确的是()
| A.生成物总能量一定低于反应物总能量 |
| B.分解反应一定是吸热反应 |
| C.应用盖斯定律,可计算某些难以直接测量的反应的焓变 |
| D.同温同压下,H2(g)+Cl2(g) |
高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能净水的处理剂。工业制备高铁酸钾的离子反应方程式为:Fe(OH)3+ C1O—+ OH—→FeO42—+C1—+ H2O(未配平)
下列有关说法不正确的是()
| A.由上述反应可知,Fe(OH)3的氧化性强于FeO42— |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为3: 2 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
某种混合气体,可能含有N2、HCl、CO。把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体体积都没有变化;再通过足量的Na2O2固体,气体体积变小;最后通过灼热的铜网,经充分反应后气体体积又减小,但还有剩余气体。下列对混合气体组成的判断,正确的是()
| A.一定没有N2,HCl和CO至少有一种 | B.一定有N2、HCl、CO |
| C.一定有N2,HCl和CO中至少有一种 | D.一定有N2与HCl,一定没有CO |
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生。下列推断正确的是( )
| A.肯定有A13+、Mg2+、Cl- | B.肯定有 A13+、Mg2+、NH4+ A13+、Mg2+、NH4+ |
| C.肯定有K+、HCO3-、MnO4- | D.肯定有A13+、Mg2+、SO42- |
用以下三种途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应。下列有关叙述不正确的是()
| A.所消耗的硝酸的量:①>②>③ |
| B.对环境造成的危害,③最小 |
| C.因铜与浓硝酸作用最快,故制取硝酸铜的最佳方案是① |
| D.三种途径所消耗的铜的质量不相等 |