常温下,下列溶液中的微粒浓度关系正确的是
| A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+) >c(OH-)=c(H+) |
| D.0.2mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=C(CH3COO-)-C(CH3COOH) |
下列各组物质分类正确的是()
| 酸 |
碱 |
盐 |
氧化物 |
|
| A |
H2SO4 |
Na2CO3 |
NaCl |
SiO2 |
| B |
HBr |
NaOH |
Na2CO3 |
CaO |
| C |
CO2 |
NH3·H2O |
NaHCO3 |
CuO |
| D |
CH3COOH |
KOH |
KCl |
HClO3 |
8月12日天津滨海新区的危险品仓库发生爆炸,遇难者上百人。以下是一些常用的危险品标志,装运乙醇的集装箱应贴的图标是()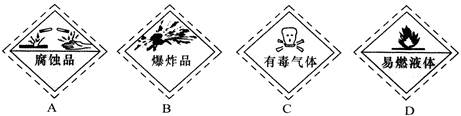
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和Cr ,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A.Cl-、Br-、Cr |
B.Cr 、Br-、Cl- 、Br-、Cl- |
C.Br-、Cl-、Cr |
D.Br-、Cr 、Cl- 、Cl- |
在0.1 mol·L-1的NaHCO3溶液中,下列关系式错误的是( )
| A.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| B.c(Na+)> c(HCO3-)>c(OH-)>c(H2CO3)> c(CO32-) |
| C.c(Na+)+c(H+)= c(HCO3-)+2 c(CO32-)+c(OH-) |
| D.c(Na+)=c(H2CO3)+ c(HCO3-)+ c(CO32-) |
下列说法正确的是( )
| A.自发反应在任何条件下都能实现 |
| B.化学反应不一定都有能量变化 |
| C.升高温度,活化分子百分数增大,化学反应速率一定增大 |
| D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |