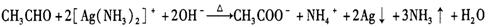NA代表阿伏加德罗常数,下列说法正确的是
A.1 L0.1 mol/L Na2CO3溶液中 和HCO—3总数为0.1 NA 和HCO—3总数为0.1 NA |
| B.22.4L氢气和4g氦气均含有NA个分子 |
| C.含2NA共价键的CnH2n+2分子的物质的量为2/(3n+l) mol |
| D.标准状况下,2.24LCl2与稀NaOH溶液反应,转移的电子总数为0.2NA |
通式为C6H5—R(R为-H、-C2H5、-OH、-SO3H、-NO2和–COOH)的6种有有机物,取等质量的6种物质分别混合于乙醚中,然后用苛性钠溶液进行萃取,振荡一段时间后,静置,能进入水层的物质有()
| A.1种 | B.2种 | C.3种 | D.4种 |
下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是()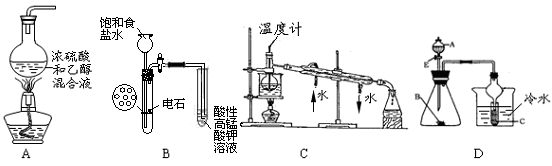
| A.实验室制乙烯 | B.实验室制乙炔并验证乙炔发生氧化反应 |
| C.实验室中分馏石油 | |
| D.若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的强弱(不考虑醋酸的挥发) |
难溶于水而且比水轻的含氧有机物是()
①硝基苯②甲苯③ 溴苯④植物油⑤蚁醛⑥乙酸乙酯⑦硬脂酸甘油酯
溴苯④植物油⑤蚁醛⑥乙酸乙酯⑦硬脂酸甘油酯
| A.②④⑥⑦ | B.①②④⑤ | C.④⑥⑦ | D.①②③ |
甘氨酸和丙氨酸混合,在一定条件下,发生缩合反应生成二肽化合物共有( )
| A.5种 | B.4种 | C.3种 | D.2种 |
下列离子方程式不正确的是
A.乙酸与碳酸钠溶液反应: |
B.醋酸溶液与新制氢氧化铜反应: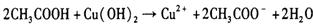 |
C.苯酚钠溶液中通入少量二氧化碳: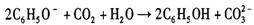 |
| D.乙醛溶液与足量的银氨溶液共热: |