36.5 g HCl溶解在1 L水中(水的密度近似为1 g/cm3),所得溶液的密度为ρg/cm3,质量分数为ω,物质的量浓度为c mol/L,NA表示阿伏加德罗常数,则下列叙述中正确的是( )
| A.所得溶液的物质的量浓度:c=1 mol/L |
| B.所得溶液中含有NA个HCl分子 |
| C.36.5 g HCl气体占有的体积为22.4 L |
| D.所得溶液的质量分数:ω=36.5 c/1 000ρ |
若以w1和w2分别表示浓度为amol/L和bmol/L氨水的质量分数,且知2 w1= w2,则下列推断正确的是
| A.2a=b | B.2b=a | C.b>2a | D.1/2b <a< b |
下列说法中错误的是
| A.从1 L 1 mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol·L-1 |
| B.制成0.5 L 10 mol·L-1的盐酸,需标况下氯化氢气体112 L |
| C.0.5 L 2 mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D.10g 98%硫酸(密度为1.84g·cm-3)与10mL 18.4 mol·L-1硫酸的浓度是不同的 |
为了配制100 mL 1 mol·L-1的NaOH溶液,其中有下列几个操作:
①NaOH固体放在纸上进行称量
②选刚用蒸馏水洗净未干燥的100 mL容量瓶进行配制
③NaOH在烧杯里刚好完全溶解,立即把溶液转移到容量瓶中
④用蒸馏水洗涤烧杯内壁2次,洗涤液也均转入容量瓶中
⑤使蒸馏水沿玻璃棒注入容量瓶,直到溶液的凹液面恰好与刻度线相切。
其中操作错误的是
| A.①②③ | B.③④⑤ | C.②③⑤ | D.①③⑤ |
除去下列溶液中的杂质(括号内为杂质),选择试剂不正确的是
| A.HNO3(HCl):用AgNO3 | B.NaOH[Ba(OH)2]:用Na2SO4 |
| C.NaCl(Na2SO4):用Ba(NO3)2 | D.KOH(K2CO3):用Ca(OH)2 |
由硫酸钾、硫酸铝和硫酸组成的混合溶液已知:c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO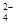 )=0.8 mol·L-1,则c(K+)为
)=0.8 mol·L-1,则c(K+)为
| A.0.15 mol·L-1 | B.0.2 mol·L-1 | C.0.3 mol·L-1 | D.0.4 mol·L-1 |