有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生。下列推断正确的是( )
| A.肯定有A13+、Mg2+、Cl- | B.肯定有A13+、Mg2+、NH4+ |
| C.肯定有K+、HCO3-、MnO4- | D.肯定有A13+、Mg2+、SO42- |
在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
| A.2 mol·L-1 | B.2.5 mol·L-1 | C.5 mol·L-1 | D.7.5 mol·L-1 |
设NA代表阿伏加德罗常数的数值。已知C2H4和C3H6的混合物的质量为a g,则该混合物( )
| A.所含共用电子对数目为(+1)NA |
| B.所含碳氢键数目为NA |
C.燃烧时消耗的O2一定是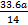 L L |
D.所含原子总数为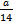 NA NA |
设阿伏加德罗常数的数值用NA表示,下列叙述中正确的是( )
①在反应KIO3+6HI KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
②35.5 g Cl2中含有共价键数为NA
③0.44 g C3H8中含有的共价键总数目为0.1NA
④24 g镁的原子中最外层电子数为NA
⑤6.4 g的S2和S8混合物中,含硫原子总数为0.2NA
⑥在常温常压下,1 mol甲烷分子所含质子数为10NA
⑦1 mol冰醋酸与1 mol乙醇在加热和浓硫酸存在条件下充分反应生成的水分子数为NA
| A.③⑤⑥ | B.②③④⑤ | C.②④⑥⑦ | D.①②③④ |
在标准状况下①6.72 L CH4②3.01×1023个HCl分子 ③13.6 g H2S④0.2 mol NH3,下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④
b.密度②>③>④>①
c.质量②>③>①>④
d.氢原子个数①>③>④>②
| A.abc | B.bcd | C.acd | D.abcd |
设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有C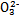 的个数为0.1NA 的个数为0.1NA |
| B.标准状况下22.4 L H2O所含分子数为NA |
| C.1 L 0.5 mol·L-1 CH3COOH溶液中,CH3COO-的个数为0.5NA |
| D.在NO、NO2的混合气体22.4 L中,含有的氮原子数为NA个 |