质量为 25.6 g的 KOH和KHCO3的混合物,先在 250℃煅烧,冷却后发现混合物的质量损失4.9g,则原混合物中KOH和KHCO3的物质的量的关系为( )
| A.KOH物质的量>KHCO3物质的量 | B.KOH物质的量<KHCO3物质的量 |
| C.KOH物质的量=KHCO3物质的量 | D.KOH和KHCO3以任意比混合 |
气体体积的大小,跟下列因素几乎无关的是
| A.分子个数 | B.温度 | C.压强 | D.分子直径 |
下列说法不正确的是
| A.在标准状况下,NA个任何分子所占的体积约为22.4L |
| B.6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14:l |
| C.在标准状况下,总质量为28g的N2和CO的混合气体,其体积约为22.4L |
| D.磷酸的摩尔质量(以g/mol为单位)与6.02×1023个磷酸分子的质量(以g为单位)在数值上相等 |
下列离子检验的方法正确的是
A.某溶液 生成白色沉淀,说明原溶液中有Cl- 生成白色沉淀,说明原溶液中有Cl- |
B.某溶液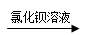 生成白色沉淀,说明原溶液中有SO42- 生成白色沉淀,说明原溶液中有SO42- |
C.某溶液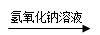 生成蓝色沉淀,说明原溶液中有Cu2+ 生成蓝色沉淀,说明原溶液中有Cu2+ |
D.某溶液 生成无色气体,说明原溶液中有CO32- 生成无色气体,说明原溶液中有CO32- |
关于下列各装置图的叙述中,不正确的是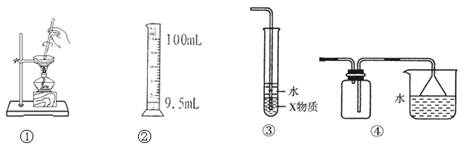
| A.装置①是把饱和食盐水中的食盐提取出来 |
| B.装置②用100mL量筒量取9.5mL液体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并可防止倒吸 |
| D.装置④可用于收集NH3,并吸收多余的NH3 |
给150mL某液体加热的操作中,所需的仪器是
①试管②烧杯③酒精灯④试管夹⑤石棉网⑥泥三角⑦坩埚⑧铁架台(带铁圈)
| A.③⑥⑦⑧ | B.②③⑤⑧ | C.①③④⑤ | D.②③⑤⑥ |