已知温度T时水的离子积常数为KW。该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a = b |
| B.混合溶液的pH = 7 |
C.混合溶液中,c(H+) = 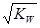 mol/L mol/L |
| D.混合溶液中,c(H+) + c(B-) = c(OH-) + c(A-) |
某离子晶体的结构(局部如图所示)中,X位于立方体的顶点,Y位于立方体的中心。请回答: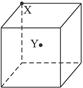
(1)该晶体的化学式为
A.X4Y B.X2YC.XY2D.XY
(2)晶体中,每个X的周围与它最接近且距离相等的X的数目为
A.4个 B.6个 C.8个 D.12个
下列物质中,含有极性键的离子化合物是
| A.CaCl2 | B.Na2O2 | C.NaOH | D.K2S |
下列物质熔化或气化时,所克服的粒子间作用力属同种类型的是( )
| A.氯化钙晶体与石墨晶体 | B.常压下0 ℃时的三氧化硫、晶体硅 |
| C.干冰、蔗糖 | D.固体氮与NaCl晶体 |
构成下列晶体的作用力相同的是( )
| A.氯化钙晶体与石墨晶体 | B.常压0 ℃时的三氧化硫、晶体硅 |
| C.干冰、蔗糖 | D.固体氮与NaCl晶体 |
关于氢键,下列说法正确的是( )
| A.在冰中每一个水分子平均可形成两个氢键 |
| B.冰、水和水蒸气中都存在氢键 |
| C.氢键属于一种化学键 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |