(10分)如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
(1)在A试管内发生反应的化学方程式是_____ ___。
(2)B装置的作用是___________________ _________。
(3)在双球干燥管内发生反应的化学方程式为________________。
(4)双球干燥管内观察到的实验现象是______________________;上述实验现象说明:________ _______________。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是:
______________________________________。
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:
(1)浓硫酸的作用是;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:
。
(2)球形干燥管C的作用是。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示);反应结束后D中的现象是
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出;再加入(此空从下列选项中选择),然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应并探讨反应所产生气体的性质。请回答下列问题:
(1)通过试管乙中发生的现象说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有性。
(2)若要收集试管甲中生成的气体,可以采用收集方法。
①排水取气法②向上排空气取气法③向下排空气取气法
(3)写出试管甲中所发生反应的化学反应方程式。
(4)试管乙口部浸有碱液的棉花的作用是,
此防范措施也说明产生的气体是气体(填“酸性”、“中性”或“碱性”)。
羟基是重要的官能团。某化学小组以下列4种物质的溶液作为研究对象,比较不同物质的羟基中氢原子的活泼性。
①碳酸 ②乙醇 ⑧苯酚 ④乙酸
I. 甲同学设计并实施了如下实验方案。
| 编号 |
实验操作 |
实验现象 |
结论及解释 |
1 |
分别取4种溶液,滴加紫色石蕊溶液 |
溶液变红的是①④溶液 |
略 |
2 |
向含酚酞的NaOH溶液中,各滴加等量的②③两种溶液 |
②中无明显现象 ③中红色明显变浅 |
滴加③时反应的化学方程式: _____________________ |
| 3 |
测定CH3COOH溶液 与H2CO3溶液的酸性 |
略 |
CH3COOH溶液的酸性远大于H2CO3溶液 |
4 |
将CO2通入C6H5ONa溶液中 |
____________ |
反应的化学方程式: ___________________ |
| 结论:4种物质的羟基中的氢原子的活泼性由强到弱的顺序是(填序号) ______________ |
II. 乙同学在研究了甲同学的实验方案后,提出如下改进方案,能一次比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如下图所示。
(1)利用上述仪器组装实验装置,其中A管插入(填字母,下同)_____中,B管插入__________中,C管插入_________中。
(2)丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有________溶液的洗气装置,使乙同学的实验设计更加完善。
为验证木炭可被浓硫酸氧化成二氧化碳,选用下图中的仪器(含所盛物质)组装成套实验装置,回答下列问题。(KMnO4能吸收SO2) 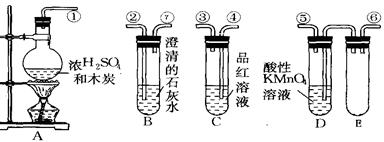
(1)在实验进行中,按气流方向从左到右的顺序,导管口的三处连接应该
是接,接,接。
(2)试管B,C中各有什么现象,才能表示已检验出二氧化碳?
B中,C中。
(3)试管D中能否用饱和NaHCO3溶液代替酸性KMnO4溶液?
说明理由:
(4)试管E的作用是
(5)写出A中反应的化学方程式:
某学生设计如下实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
(1)A仪器的名称是,所盛试剂是。
(2)漂白粉将在U型管中产生,其化学反应方程式是。
(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是。
(4)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是。