下列表示对应化学反应的离子方程式正确的是( )
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O===3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-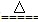 NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O===HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-===Ag++NO↑+H2O |
下列各组原子,彼此性质一定相似的是( )
| A.1s2与2s2的元素 |
| B.M层上有两个电子与N层上有两个电子的元素 |
| C.2p上有一个未成对电子与3p上有一个未成对电子的元素 |
| D.L层上有一个空轨道和M层的p轨道上有一个空轨道的元素 |
下列关于丙烯(CH3—CH =CH2)的说法正确的是( )
| A.丙烯分子有8个σ键,1 个π键 |
| B.丙烯分子中3个碳原子都是sp3杂化 |
| C.丙烯分子不存在非极性键 |
| D.丙烯分子中3个碳原子可能在同一直线上 |
某有机物的结构简式如图所示,关于该物质的叙述错误的是()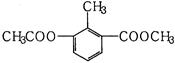
| A.一个分子中含有12个H原子 |
| B.能使酸性KMnO4溶液褪色 |
| C.苯环上的一氯代物有2种 |
| D.1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol |
、断肠草为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构式,下列推断不正确的是( )
虎茸草素异虎耳草素异佛手相内酯 6-甲氧基白芷素
①②③④
| A.①与②、③与④分别互为同分异构体 |
| B.①、③互为同系物 |
| C.等物质的量②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者多 |
| D.①、②、③、④均能与氢氧化钠溶液反应 |
某分子式为C10H20O2的酯,在一定条件下可发生如下图的转化过程:则符合上述条件的酯的结构可能有()
| A.2种 | B.8种 | C.6种 | D.4种 |