某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是( )
| A.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
| B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| D.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
乙醇的燃烧热为ΔH1,甲醇的燃烧热为ΔH2,且ΔH1<ΔH2,若乙醇和甲醇的混合物1 mol完全燃烧,反应热为ΔH3,则乙醇和甲醇的物质的量之比为 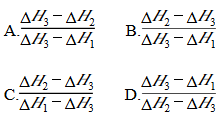
在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+3/2O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=3/2S2(g)+2H2O(g)△H2
③H2S(g)+1/2O2(g)=S(g)+H2O(g)△H3
④2S(g)=S2(g)△H4
则△H4的正确表达式为
| A.△H4=2/3(△H1+△H2-3△H3) | B.△H4=2/3(3△H3-△H1-△H2) |
| C.△H4=3/2(△H1+△H2-3△H3) | D.△H4=3/2(△H1-△H2-3△H3) |
反应C(s)+H2O(g) CO2(g)+H2(g)在一可变容积的密闭容器中进行,下列条件改变对其反应速率几乎无影响的是
CO2(g)+H2(g)在一可变容积的密闭容器中进行,下列条件改变对其反应速率几乎无影响的是
| A.增加水蒸气的量 | B.将容器的体积缩小一半 |
| C.保持体积不变,充入N2 | D.压强不变,充入N2使体积增大 |
下表中是各组反应的反应物和温度,反应刚开始时,放出H2速率最快的是
| 金属(粉末状)(mol) |
酸的浓度及体积 |
反应温度(℃) |
|
| A |
Mg 0.1 |
0.1 6 mol·L-1硝酸10mL |
80 |
| B. |
Mg 0.1 |
0.1 3 mol·L-1盐酸10mL |
60 |
| C. |
Fe 0.1 |
0.1 3 mol·L-1盐酸10mL |
60 |
| D. |
Mg 0.1 |
0.1 3 mol·L-1硫酸10mL |
60 |
下列说法不正确的是
| A.反应物的分子的每次碰撞都能发生化学反应 |
| B.反应物分子(或离子)间的每次碰撞是反应的先决条件 |
| C.参加反应的物质的性质是决定化学反应速率的重要因素 |
| D.活化分子具有比普通分子更高的能量 |