下列表示对应化学反应的离子方程式正确的是( )
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O===3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O===HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-===Ag++NO↑+H2O |
下列有关溶液组成的描述合理的是
| A.常温下在c(H+)=1×10-13mol/L的溶液中能大量存在Mg2+、Cu2+、SO42-、NO3 |
| B.使甲基橙试液变红的溶液中可能大量存在Na+、ClO‾、SO42‾、I‾ |
C.使PH试纸变蓝的溶液中可大量存在Na+、K+、AlO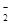 、CO 、CO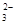 |
| D.常温下,在水电离产生的c(H+)×c(OH-)=1×10-24的溶液中可大量存在Fe2+、Cl-、NO3-、K+ |
下列试剂的保存方法正确的是
| A.氢氟酸保存在玻璃瓶中 ,烧碱溶液存放在带有玻璃塞的试剂瓶中 |
| B.水玻璃存放在滴瓶中,硝酸银溶液保存在无色广口瓶中。 |
| C.少量金属钠保存在煤油中,少量白磷保存在水中。 |
| D.液溴直接存放在棕色滴瓶中,浓硝酸保存在带橡胶塞的无色玻璃瓶中。 |
下列说法不正确的是
| A.铜片在稀硫酸和NaNO3混合溶液中可溶解 |
| B.常温常压下,46gNO2和N2O4混合气体共含有3mol原子 |
| C.光纤通讯中制造光纤的基本原料是SiO2 |
| D.光照氯水有气泡逸出该气体是Cl2 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.78g 苯含有C=C双键的数目为3NA |
| B.室温下,1LpH=13的Ba(OH)2溶液中,溶液中的OH-离子数目为0.2NA |
| C.0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA |
| D.含2molH2SO4的浓硫酸与足量铜片在加热条件下反应,产生NA个SO2气体分子 |
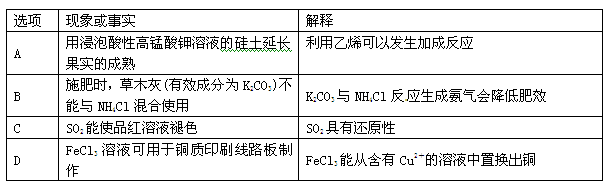
化学与社会、生活密切相关。对下列现象或事实的解释正确的是