(5分)实验室常用饱和亚硝酸钠与氯化铵溶液反应制取纯净的氮气。反应的化学方程式为:NaNO2+NH4Cl=NaCl+N2+2H2O(此反应是放热反应),实验装置如图4所示。试回答: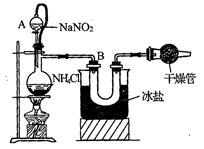
(1)装置中A部分的分液漏斗与蒸馏瓶之间连接的导管所起的作用是 (填编号)
A.防止NaNO2饱和溶液蒸发
B.保证实验装置不漏气
C.使NaNO2饱和溶液容易滴下
(2)B部分的作用是 (填编号)
A.冷凝
B.冷却氮气
C.缓冲氮气流
(3)加入药品前必须进行的一个实验步骤是 ,加热片刻后,即应移去酒精灯以防反应物冲出,其原因是
(4)收集N2最适宜的方法是 (填编号)
A.用排气法收集在集气瓶中
B.用排水法收集在集气瓶中
C.直接收集在气球或塑料袋中
研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验。
实验一:比较两种物质的热稳定性
设计如右图装置:小试管套装在带有支管的大试管中,整套装置气密性好,其他装置略去。
(1)为确保安全,实验结束时,在移离酒精灯前必须完成的操作是。
(2)现象与结论:装有碳酸氢钠的试管口生成较多的无色小液滴,同时试管A中有大量的气泡产生,澄清石灰水变浑浊;试管B中也有气泡产生,澄清石灰水没有明显的变化;实验结束后,经检验大、小两试管内的物质均是碳酸钠。结合以上实验,可得出结论:①碳酸氢钠受热生成的物质是碳酸钠、和。
②在受热条件下,碳酸钠比碳酸氢钠稳定。
(3)反思与讨论:加热大试管时,碳酸钠的受热温度会高于碳酸氢钠。这能否准确地说明"在受热条件下,碳酸钠比碳酸氢钠稳定"这一结论?(填"能"或"否"),理由是。
实验二:比较与盐酸反应生成相同体积二氧化碳气体的快慢
取碳酸氢钠4.2 g放入如图Ⅰ装置的锥形瓶中,取碳酸钠5.3 g放入另一相同装置的锥形瓶中,分别加入相同质量、相同浓度的盐酸(足量)。相同的条件下,通过图Ⅱ装置测量出生成气体的体积,得到时间-体积关系曲线如图Ⅲ所示。


图Ⅰ图Ⅱ图Ⅲ
(4)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是。
(5)数据与分析:根据图Ⅲ曲线,可得出有关"比较与盐酸反应生成相同体积二氧化碳气体的快慢"的结论是。
(6)反思与讨论:实验中 "取碳酸氢钠4.2
、碳酸钠5.3
"的目的是。
用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方 法。实验过程是:
法。实验过程是: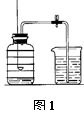
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,立即伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。
请回答下列问题:
(1)上面的实验同时证明了氮气有的化学性质。
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是 ___________。(至少二点)
(3)某同学对实验进行反思后,提出了改进方法(如图2所示 ),你认为改进后的优点是: ________________。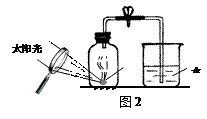
下图是实验室中用于制取、干燥和收集气体的装置图。实验课上同学们用过氧化
氢溶液与二氧化锰混合制取并收集氧气,试回答:
(1)用该方法制取氧气的化学表达式是_____________________________________。
(2)该方法制取氧气的发生装置应选择__________ _。
_。
(3)甲、乙、丙三名同学用所选装置合作实验过程中,胶塞突然弹飞,并有少量的液体溅到实验台和衣服上。就此异常现象三名同学探究如下:
【问题】为什么胶塞会突然弹飞呢?
【查阅资料】①容器内瞬间产生气体过多,压强过大,可能导致胶塞弹飞。
②化学反应速率与反应物的浓度、接触面积、温度、催化剂等因素有关。
【猜想】甲同学:导气管堵塞或弯折造成的。
乙同学:过氧化氢溶液用量过多造成的。
丙同学:过氧化氢溶液的溶质质量分数过大造成的。
【分析验证】通过检查实验装置发现导气管没有堵塞、弯折的情况;与实验成功的小组同学交流,得知各小组所用过氧化氢溶液溶质的质量分数均相同。于是他们否定了_________________两名同学的猜想。请你设计实验,验证另一名同学的猜想是导致本次实验胶塞弹飞的主要原因。
【交流反思】①老师建议他们可以通过改进发生装置的方法,避免胶塞弹飞。你对所选的发生装置有何改进设想?(语言叙述或画图均可)
②实验结束后,有的同学发现衣服和手上出现有白色的斑点,手上还微微发痛。由此联想到过氧化氢溶液还可能具有性。
为了探究“水的净化”过程,某实验小组从河中取了水样,观察到:
A. 水样呈黄色,有异味 B.水样浑浊,有固体小颗粒。
现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒,在此操作中,玻璃棒所起的作用是。
再向滤液中加入活性炭,利用其性除去水样中的颜色和异味,该过程属于
变化(填“物理”或“化学”)
(2)若过滤结束,发现滤液仍然浑浊,可能的原因是
①②。
(3)同学们想知道所得滤液中是否溶解了某些固体物质,可接着对滤液进行(填
操作方法)。
实验室现有下列仪器和用品,要进行该操作,必须用到的是(填序号)。
①试管 ②铁架台(带铁圈) ③烧杯④酒精灯 ⑤滤纸 ⑥玻璃棒 ⑦量筒 ⑧蒸发皿
某同学用下图所示实验装置对质量守恒定律进行探究。请回答: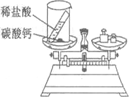
(1)反应前,托盘天平的指针指向刻度盘的中间;那么,两种物质反应后,托盘天平的指针(填"发生"或"不发生")偏转。
(2)你认为该同学的探究活动能否验证质量守恒定律?。
(3)如果你进行该探究活动。装置不变,你选用什么药品?。药品不变,你选用怎样的装置?。