某温度下,浓度都是1 mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,达到平衡后X2为0.4 mol/L,Y2为0.8mol/L,生成的Z为0.4mol/L ,则该反应式是
A.X2 + 2Y2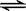 2XY2 2XY2 |
B.2X2 + Y2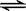 2X2Y 2X2Y |
C.3X2 + Y2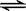 2X3Y 2X3Y |
D.X2 + 3Y2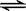 2XY3 2XY3 |
实验室中某些气体的制取、收集及尾气处理装置如图所示。仅用此装置和表中提供的物质完成相关实验,最合理的是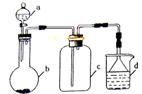
| 选项 |
a中物质 |
b中物质 |
c中收集的气体 |
d中物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
Na2SO3 |
SO2 |
NaOH溶液 |
| C |
饱和食盐水 |
电石 |
CH≡CH |
H2O |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
下列鉴别方法不可行的是
| A.用水鉴别乙醇、甲苯和溴苯 |
| B.用KMnO4(H+)溶液鉴别苯、环已烯和环已烷 |
| C.用燃烧法鉴别乙醇、苯和四氯化碳 |
| D.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
NA代表阿伏加德罗常数。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,对该反应的分析,错误的是
| A.反应前后物质中阴、阳离子数目保持不变 |
| B.反应前后总物质的量减少0.5mol |
| C.反应中转移了NA电子并生成了11.2L氧气 |
| D.反应的二氧化碳和生成的氧气体积比为2:1 |
CO(g)+H2O(g) CO2(g)+H2(g)+Q,将1molCO和1molH2O置于密闭容器中发生上述反应,其他条件不变的情况下,下列叙述正确的是
CO2(g)+H2(g)+Q,将1molCO和1molH2O置于密闭容器中发生上述反应,其他条件不变的情况下,下列叙述正确的是
| A.加入催化剂,改变了反应的途径,反应放出的热量也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.若将该反应设计成原电池,反应放出的热量不变 |
一种新催化剂,能在室温下催化空气氧化甲醛:HCHO+O2 CO2+H2O,该反应
CO2+H2O,该反应
| A.反应物和生成物中都含极性分子和非极性分子 |
| B.生成1.8gH2O消耗2.24L O2 |
| C.反应时有极性键和非极性键的断裂和它们的生成 |
| D.为吸热反应 |