在两个恒容容器中有平衡体系:A(g) 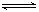 2B(g)和2C(g)
2B(g)和2C(g) 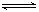 D(g),X1和X2分别是A和C的转化率。在温度不变时分别增加相同物质的量的A和C。下列判断正确的是( )
D(g),X1和X2分别是A和C的转化率。在温度不变时分别增加相同物质的量的A和C。下列判断正确的是( )
A.X1降低,X2增大 B.X1、X2均降低 C.X1增大,X2降低 D.X1、X2均增大
某物质的水溶液能导电,且该物质属于非电解质,溶于水化学键被破坏的是
| A.液溴 | B.干冰 | C.蔗糖 | D.硫酸钡 |
下列说法不正确的是
| A.Na2O2、HClO、SO2等物质都具有漂白作用 |
| B.液氨、液氯、液态氯化氢都是电解质 |
| C.所有的置换反应都是氧化还原反应,而所有的复分解反应都是非氧化还原反应 |
| D.非金属氧化物不一定是酸性氧化物,有些金属氧化物也能与强碱反应 |
2012年3月新修订的《环境空气质量标准》增设了PM 2.5(直径小于或等于2.5微米的颗粒物)浓度限值、臭氧8小时平均浓度限值。下列有关说法正确的
| A.PM 2.5所指颗粒物大小与胶体中分散质粒子大小相当 |
| B.O2和O3互为同素异形体,两者的化学性质相同 |
| C.O3转化为O2和O2转化为O3过程中均有能量变化 |
| D.反应3O2=2O3有单质参加,属于氧化还原反应 |
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是
| A.煤经过气化和液化两个物理变化,可变为清洁能源 |
| B.服用铬含量超标的药用胶囊会对人体健康造成危害 |
| C.以NO和NO2为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因 |
| D.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应。下列有关说法正确的是( )
| A.反应后溶液中Fe3+物质的量为0.8mol |
| B.反应后产生13.44L H2(标准状况) |
| C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol |
| D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体 |