已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A.该溶液的pH=4 |
| B.升高温度,溶液pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
在0.1 mol·L-1的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+。对于该平衡,下列叙述正确的是
CH3COO-+H+。对于该平衡,下列叙述正确的是
| A.加水,反应速率增大,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.滴加少量0.1 mol·L-1HCl溶液,溶液中c(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
下列事实不能用化学平衡原理解释的是
| A.温度控制在500℃有利于合成氨反应 |
| B.用排饱和食盐水法收集Cl2 |
| C.打开碳酸饮料会有大量气泡冒出 |
| D.在硫酸工业生产中使用过量的氧气 |
关于平衡常数,下列说法不正确的是
| A.平衡常数随温度的改变而改变 |
| B.使用催化剂不能改变平衡常数 |
| C.平衡常数不随反应物或生成物浓度的改变而改变 |
| D.增大压强促使平衡向正反应方向进行,则平衡常数增大 |
恒容容器中反应:A(g)+3B(g) 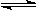 2C(g)+3D(g),达到平衡的标志是
2C(g)+3D(g),达到平衡的标志是
①体系的压强不再改变②混合气体的平均相对分子质量不再改变③各组分的浓度不再改变④混合气体的密度不变⑤反应速率vA: vB: vC: vD=1:3:2:3⑥单位时间内1 mol A断键反应,同时2 mol C也断键反应
| A.②③⑤⑥ | B.②③④⑤ | C.①④⑤⑥ | D.①②③⑥ |
对于A2+3B2 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
A.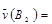 0.8mol·L-1·s-1 0.8mol·L-1·s-1 |
B.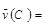 0.7mol·L-1·s-1 0.7mol·L-1·s-1 |
C.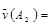 0.4mol·L-1·s-1 0.4mol·L-1·s-1 |
D.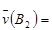 54mol·L-1·min-1 54mol·L-1·min-1 |