已知氢氧化钠和氢氧化钡混合溶液的 PH =" 14," 现取 100mL该混合溶液, 加入100mL0.4mol/LH2SO4溶液时生成的沉淀已达最多(溶液的体积变化忽略不计), 计算回答下列问题:(无计算过程不得分)
(1)原混合溶液中氢氧化钠和氢氧化钡的物质的量浓度为多少?
(2)反应后所得溶液的PH为多少?
6.0 g某有机物A完全燃烧后,生成标况下的CO2 6.72 L和7.2 g H2O,测得该化合物的蒸气对氢气的相对密度是30,求该化合物的分子式。
(8分)为了测定一种气态烃A的化学式,取一定量的A置于一密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的最简式,他们测得的在一定条件下的有关数据如下(图中的箭头表示气流的方向,实验前系统内的空气已排尽):
甲方案:燃烧产物浓硫酸增重2.52 g碱石灰增重1.30 g生成CO21.76 g
乙方案:燃烧产物碱石灰增重5.60 g固体减小0.64 g石灰水增重4 g。试回答:
(1)甲、乙两方案中,你认为哪种方案能求出A的最简式?
(2)请根据你选择的方案,通过计算求出A的最简式。
(3)若要确定A的分子式,是否需要测定其它数据?并说明原因。
已知某有机物X有如下性质:①X的蒸气对H2的相对密度为31.0;②取12.4gX与过量的金属钠完全作用后,生成4480mL(标准状况)气体;③取等质量的X完全燃烧后,产生的气体依次通过浓硫酸和碱石灰,使两者的质量分别增加10.8g和17.6g。求X的结构简式。
12.0 g某液态有机化合物A完全燃烧后,生成14.4 g H2O和26.4 gCO2。测得有机化合物A的蒸气对H2的相对密度是30,求: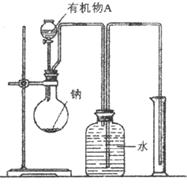
(1)有机物A的分子式。
(2)用如图所示装置测定有机物A的分子结构,实验数据如下(实验数据均已换算为标准状况):a mL(密度为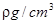 )的有机物A与足量钠完全反应后,量筒液面读数为b mL,若1 molA分子中有x mol氢原子能跟金属钠反应,则x的计算式为(可以不化简)。
)的有机物A与足量钠完全反应后,量筒液面读数为b mL,若1 molA分子中有x mol氢原子能跟金属钠反应,则x的计算式为(可以不化简)。
某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。
(1)求该有机物的分子式?
(2)实践中可根据核磁共振氢谱(PMR)上观察到氢原子给出的峰值情况,确定有机物的结构。此含有苯环的有机物,在PMR谱上峰给出的稳定强度仅有四种,它们分别为:① 3∶1∶1②1∶1∶2 ∶6③3∶2④3∶2∶2∶2∶1 ,请分别推断出其对应的结构:
①;②;
③;④。