由化学能转变的热能或电能仍然是人类使用的主要能源.根据下图所示的装置,判断下列说法不正确的是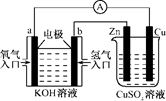
| A.该装置中Cu极为阳极 |
| B.当铜片的质量变化了12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
| C.该装置中b极的电极反应式是:H2+2OH--2e-===2H2O |
| D.该装置中a极为正极,发生氧化反应 |
在可逆反应中,改变下列条件一定能加快反应速率的是()。
| A.增大反应物的量 | B.升高温度 |
| C.增大压强 | D.使用催化剂 |
将Mg条投入盛有稀HCl的容器里,产生H2的速率与下列因素:①盐酸浓度②温度③镁条的表面积④容器的密闭情况⑤溶液中c(Cl-)大小,有关系的是()。
| A.①② | B.③④ | C.①②③④ | D.①②③④⑤ |
在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(mol·L-1·s-1)表示,且υ(A)、υ(B)、υ(C)之间有如下所示的关系: υ(B)=3υ(A);3υ(C)=2υ(B)。则此反应可表示为()。
A、2A+3B=2CB、A+3B=2CC、3A+B=2CD、A+B=C
对于在一密闭容器中进行如下反应:C(S)+O2(g)=CO2(g)下列说法错误的是()。
| A.将木炭粉碎成粉末状可以加快化学反应速率 |
| B.升高温度可以加快化学反应速率 |
| C.增加压强可以加快化学反应速率 |
| D.增加木炭的量可以加快化学反应速率 |
25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是ΔH=-393.5kJ/mol、ΔH=-285.8kJ/mol、ΔH=-890.3kJ/mol、ΔH=-2800kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+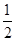 O2(g)===CO(g)ΔH=-393.5kJ/mol O2(g)===CO(g)ΔH=-393.5kJ/mol |
| B.2H2(g)+O2(g)===2H2O(g)ΔH=+571.6kJ/mol |
| C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-890.3kJ/mol |
D.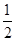 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l)ΔH=-1400kJ/mol C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l)ΔH=-1400kJ/mol |