下列关于化学反应的描述中正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.反应4Fe(OH)2(s) +02(g)+2H20(l)=4Fe(OH)3(S)的△H>O |
C.已知①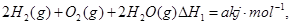 ② 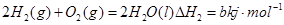 ,则a<b ,则a<b |
| D.CO(g)的标准燃烧是283.0kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)△H=+566.0kJ·mol-1 |
下列物质能使紫色石蕊试液由紫变红又褪色的是
①Cl2②盐酸③氯水④盐酸酸化的漂白粉溶液⑤木炭⑥Na2O2
| A.①②③⑥ | B.①③④ | C.②③④ | D.①③④⑤⑥ |
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16. 9 g过氯化钡(BaO2)固体中阴、阳离子总数约为0. 2NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
| C.a g某气体含分子数为b,c g该气体在标况下的体积为22. 4bc/ aNAL |
| D.某密闭容器盛有0. l molN2和0. 3 mol H2,在一定条件下充分反应,转移电子的数目为0. 6NA |
下列有关双氧水说法错误的是
| A.H2O2、Na2O2都属于过氧化物,都存在共价键 |
| B.双氧水是绿色氧化剂,可作医疗消毒剂 |
| C.H2O2在过氧化氢酶的催化下,温度越高,分解速率越快 |
| D.H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似,与SO2不同 |
能正确表示下列反应的离子方程式是
| A.硫酸铝溶液中加入过量氨水:Al3++3OH—=Al(OH)3↓‘ |
| B.碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32—=CaCO3+2OH— |
| C.冷的氢氧化钠溶液中通入氯气:Cl2+2OH—=ClO-+Cl—+H2O |
| D.稀硫酸中加人铁粉:2 Fe+6H+=2Fe3++3H2↑ |
下列溶液中能够区别SO2和CO2气体的是
①澄清石灰水②KMnO4酸性溶液 ③氯水④品红溶液
| A.①③④ | B.②③④ | C.①②③ | D.全部 |