丙烯与某气态烃组成的混合气完全燃烧时,所需氧气的体积是混合气体体积的5倍(相同状况),则该气态烃是( )
| A.C4H8 | B.C3H4 | C.C2H6 | D.C2H4 |
石墨由多“层”构成,质地柔软,但分离成一“层”后即成为“石墨烯”,硬度超过了金刚石,导电能力也大大超过了一般的导体,这再次验证了
| A.量变引起质变的规律 | B.能量守恒与转换的规律 |
| C.勒夏特列原理 | D.阿伏加德罗定律 |
苹果联建公司用价格更低的正己烷代替酒精清洗电器零部件,已造成许多工人中毒。关于正己烷的叙述错误的是
| A.分子式为C6H14 | B.属芳香烃 | C.有毒 | D.易挥发 |
1.卢瑟福的α粒子散射实验的现象不能说明
| A.原子中原子核占的体积很小 | B.原子是可以再分的 |
| C.原子中存在着带正电荷的核 | D.核外电子象行星一样围绕原子核运动 |
与下列图像有关的说法正确的是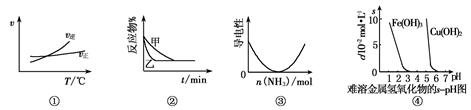
A.根据图①可判断A2(g)+3B2(g) 2AB3(g)的ΔH>0 2AB3(g)的ΔH>0 |
B.图②表示压强对2A(g)+B(g) 3C(g)的影响,甲的压强大 3C(g)的影响,甲的压强大 |
| C.图③表示乙酸溶液中通入氨气后溶液导电性的变化 |
| D.根据图④,调节溶液的pH 为4即可除去CuSO4溶液中的Fe3+ |
常温时,下列关于溶液的pH或微粒的物质的量浓度的说法不正确的是
A.pH = 3的二元弱酸H2R溶液与pH = 11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液中:2c ( R2+ ) + c ( HR- ) =" c" ( Na+ )
B.某溶液中只存在Cl-、OH-、NH4+、H+四种离子,则一定不存在下列关系:
c ( Cl- ) > c ( NH4+ ) > c ( H+ ) =" c" ( OH- )
C.某物质的溶液中由水电离出的c ( H+ ) = 1×10-a mol·L-1,若a > 7,则溶液的pH一定为14 - a
D.将0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液中:2c( OH- ) + c( A- ) ="2c(" H+ ) + c( HA )