A—J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知
A是一种高熔点物质,B为空气的成分之一,D是一种红棕色固体。请回答下列问题:
(1)固体A的晶体类型为___________,K的化学式为 。
(2)C与D在高温下的反应在冶金工业上称为 反应,引发该反应的实验操作是
(3)G→J的化学方程式为____________。
(4)A→H的离子方程式为 。
(5)I的水溶液pH_____7(填“>”、“<”或“=”),原因是____________(用离子方程式表示)。
I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是腐蚀(填“析氢”或“吸氧”)。
(2)写出铁锅腐蚀正极的电极反应式:
II.①某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:
Cu+H2SO4(稀)=CuSO4+H2↑。
请在答题卡上画出能够实验这一反应的装置图,并在图中进行必要的标注。
②某同学在做一定条件下铜与稀硫酸的反应实验时,看到碳棒上有气泡产生,但铜棒却没有被腐蚀。请你分析其原因:
已知[Ksp(AgBr) ]=5.4×10-13,[Ksp(AgCl) ]=2.0×10-10。
(1)向浓度均为0.1mol·L-1的KBr、NaCl混合溶液中滴入0.1mol·L-1的AgNO3溶液,首先生成的沉淀是。
(2)当容器中同时出现AgCl和AgBr沉淀,溶液中c(Br-)/c(Cl-)=。
某溶液经检测只含有NH4+、Cl-、H+、OH-四种离子,
(1)若该溶液中只有一种溶质,则该溶质是(写化学式)。
(2)若该溶液呈中性,则溶液中c(NH4+)c(Cl-)(填“>”、“<”或“=”),此时溶液中的溶质有。
(3)若该溶液由0.02mol·L-1HCl与0.01mol·L-1NH3·H2O等体积混合而成,则溶液中四种离子的浓度由大到小的顺序为。
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如右下图所示装置。试回答下列问题: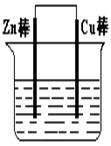
|
X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收。已知X是化石燃料燃烧的产物之一,是形成酸雨的主要物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应。请写出下列反应的方程式。
(1)X在一定条件下与氧气的反应方程式。
(2)Y与氢氧化钠溶液的离子反应方程式。
(3)Z与水的反应方程式。