欲除去硝酸钾固体中混有的少量氯化钾杂质,某学生进行如下实验操作。回答下列问题:
⑴溶解样品。该过程所需的仪器有 。
⑵向溶解后的溶液中加入适量的 溶液,使氯化钾转化为 沉淀。(填化学式)
⑶将混合液进行过滤,过滤装置和操作如图所示,指出图中的两处错误: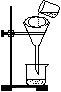
① ;
② 。
现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了鉴别四种溶液各是什么,将它们随意编号为A、B、C、D后,按下表进行实验,产生的现象如下表所示。
试根据实验现象回答:
| 实验顺序 |
实验内容 |
实验现象 |
| ① |
A+B |
没有现象发生 |
| ② |
B+D |
有气体放出 |
| ③ |
C+B |
有沉淀生成 |
| ④ |
A+D |
有沉淀生成 |
(1)推断并写出各物质的化学式:
A、B、C、 D。
(2)写出各序号实验中有关反应的离子方程式,不反应的说明理由。
①
②
③
④
如图所示,在一烧杯中盛有H2SO4溶液, 同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入与H2SO4溶液同浓度的Ba(OH)2溶液至恰好完全反应。试回答下列问题:
同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入与H2SO4溶液同浓度的Ba(OH)2溶液至恰好完全反应。试回答下列问题: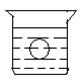
 (1)该实验中,观察到的现象有
(1)该实验中,观察到的现象有
①,
②。
(2)写出该实验中反应的离子方程式
。
[有机化学基础]苯酚是重要的化工原料,通过下列流程可合成阿司匹林、香料和一些高分子化 合物。已知:
合物。已知:
(1)写出反应类型:④__________________,A中含有官能团的名称。
(2)写出C的结构简式____________________,G的结构简式_____________________。
(3)写出反应B与氢氧化钠反应的化学方程式___________________________________________。
(4)写出反应②的化学方程式______________________________________________。
(5)写出反应⑧的化学方程式_______________________________________________。
(6)下列可检验阿司匹林样品中混有水杨酸的试剂是__________。
(a)三氯化铁溶液(b)碳酸氢钠溶液(c)石蕊试液
(7)保持官能团和位置不变,写出B的同分异构体有种
可逆反应N2+3H2 2NH3是工业上合成氨的重要反应。

图1 (图中表示生成1mol物质时的能量) 图2
(1)根据图1请写出合成氨的热化学方程式(热量用E1、E2或E3表示)
(2)图1中虚线部分是通过改变化学反应中的条件,请解释原因
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率与反应过程的关系,其中表示平衡混合物中NH3的含量最高的一段时间是
(4)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是(“正向移动”“ 逆向移动”或“不移动”)
(5)将上述实验中产生的NH3通入到0.04mol·L-1的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为(已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38)
已知:在实验中,常常利用高沸点酸制低沸点酸。以六水合氯化镁(MgCl2·6H2O)为原料制备无水氯化镁。已知MgCl2·6H2O晶体在空气中加热时,释放出部分结晶水,同时生成Mg(OH)Cl或MgO;在干燥HCl气流中加热,能制得无水MgCl2。
可选用药品:MgCl2·6H2O晶体、NaCl(s)、KClO3(s)、MnO2、浓H2SO4、浓盐酸、稀NaOH溶液。 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题: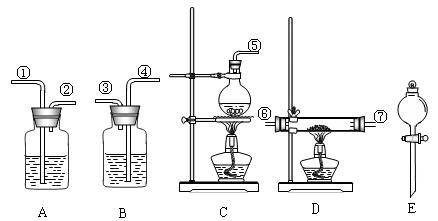
(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B等填入)是,
有关的化学方程式是。
(2)按气流方向,其余装置的连接顺序(用数字①、②等填入)是:
()→()()→()()→()()
(3)各装置中应放的药品: B.______,D.______,E.______。
(4)B装置的作用是_________________。
(5)从实验安全角度考虑,上述所给药品和仪器设计的实验存在不足,请你提出修改建议:。