二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
(1)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g)的ΔH= ___________;
CH3OCH3(g) + CO2 (g)的ΔH= ___________;
(2)已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
①比较此时正、逆反应速率的大小:v正 ______ v逆(填“>”、“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) = _________;该时间内反应速率v(CH3OH) = __________。
(3)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 、
、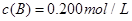 及
及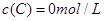 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。
请回答下列问题:
与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②_______________;______________________________________________;
③_______________________________________________;
该反应的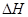 _________0,判断其理由是__________________________________;
_________0,判断其理由是__________________________________;
按要求书写下列方程式。
① NaHCO3溶液的电离方程式:。
② H2S溶液的电离方程式:。
③ NH4NO3溶液的水解离子方程式:。
④ Na2CO3溶液的水解离子方程式:。
物质的量浓度相同、体积相同的HCl、H2SO4、CH3COOH等三种溶液,
(1)三种溶液中氢离子浓度最大的是。
(2)分别用0.1mol/L的NaOH溶液中和,其中消耗NaOH溶液最多是。
已知某反应2A B + C在某一温度时,达到平衡。
B + C在某一温度时,达到平衡。
(1)若升高温度时,平衡向正反应方向移动,则正反应是热反应;
(2)若减少压强时,平衡向正反应方向移动,则A呈态;
(3)若该反应达到平衡时,加入一定量的B物质,平衡将会向逆反应方向移动,则B的转化率,C的转化率。
雷雨中常含有微量的硝酸,对农作物生长有利,试用化学方程式解释硝酸的形成过程:
①;② ;③。
;③。
氮族元素属于第族,原子核外最外层电子数为,最高价氧化物的通式为,其氢化物通式为,随核电荷数的递增,氢化物的稳定性逐渐。