Li-SOCl2电池可用于心脏起搏器。电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl +S +SO2。电池工作时,下列说法不正确的是
| A.锂电极发生氧化反应 |
| B.电子从锂电极通过外电路流向碳电极 |
| C.每生成1mol SO2转移4mol电子 |
| D.SOCl2既是氧化剂又是还原剂 |
下列有机物命名正确的是()
A.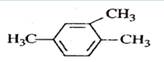 1,3,4-三甲苯 1,3,4-三甲苯 |
B.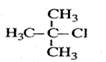 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 |
C.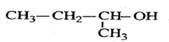 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D. 2-甲基-3-丁炔 2-甲基-3-丁炔 |
下列各组物质不属于同分异构体的是 ( )
| A.2,2一二甲基丙醇和2一甲基丁醇 | B.邻氯甲苯和对氯甲苯 |
| C.2一甲基丁烷和戊烷 | D.甲基丙烯酸和甲酸丙酯 |
BaCl2有剧毒,致死量0.3g,万一不慎误服,应大量吞服鸡蛋清及适量的解毒剂,此解毒剂应是()
| A.AgNO3 | B.CuSO4 | C.MgSO4 | D.NaCl |
下列化合物中既能使溴的四氯化碳溶液褪色,又能在光照下与溴发生取代反应的是
| A.甲苯 | B.乙醇 | C.丙烯 | D.乙烯 |
下列有关物质的表达式不正确的是
| A.2—甲基—1,3—丁二烯的分子式:C5H8 |
B.溴乙烷的电子式: |
C.甲醛的结构式: |
| D.果糖的结构简式:CH2OH(CHOH)3COCH2OH |