下列实验过程中出现的异常情况,其可能原因分析错误的是( )
| 选项 |
异常情况 |
可能原因分析 |
| A |
蒸发结晶:蒸发皿破裂 |
将溶液蒸干或酒精灯灯芯碰到热的蒸发皿底部 |
| B |
分液:分液漏斗中的液体难以滴下 |
没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
| C |
蒸馏:冷凝管破裂 |
冷凝管没有通水或先加热后通水 |
| D |
萃取:液体静置不分层 |
加入萃取剂的量较多 |
“化学与社会、生活、科研密切的关系”。下列叙述中,不正确的是
| A.大量使用燃煤发电是形成雾霾的主要原因 |
| B.天然气、煤气大量泄漏遇到明火会爆炸 |
| C.利用化学反应可实现12C到14C的转化 |
| D.晶体硅可用于光伏发电、制造芯片 |
A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液中的一种,已知A、B溶液的pH相同,A、C溶液混合后溶液变浑浊。下列说法正确的是
A.D溶液的pH<7
B.C溶液中的溶质溶于水促进了水的电离
C.溶液A滴入到碳酸氢钠溶液中产生气体
D.溶液B进行焰色反应呈黄色
下列关系的表述中,正确的是
A.0.1mol·L-1NaHSO4溶液中:c(Na+)+c(H+)=c( )+c(OH-) )+c(OH-) |
| B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1:1 |
| C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等 |
D.0.1mol·L-1NaHCO3溶液中:c(Na+)>c(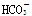 )>c( )>c(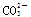 )>c(H2CO3) )>c(H2CO3) |
用0.10mol·L-1的盐酸滴定0.10mol·L-1的氨水,滴定过程中不可能出现的结果是
A.c(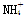 )>c(Cl-),c(OH-)>c(H+) )>c(Cl-),c(OH-)>c(H+) |
B.c(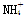 )=c(Cl-),c(OH-)=c(H )=c(Cl-),c(OH-)=c(H |
C.c(Cl-)>c(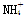 ),c(OH-)>c(H+) ),c(OH-)>c(H+) |
D.c(Cl-)>c(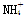 ),c(H+)>c(OH-) ),c(H+)>c(OH-) |
可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应
①Br2 + 2e-= 2Br-②2Br- - 2e-= Br2③Zn – 2e-= Zn2+④Zn2+ + 2e-= Zn其中表示充电时的阳极反应和放电时的负极反应的分别是
| A.②和③ | B.②和① | C.③和① | D.④和① |