用下图所示装置进行下列实验,实验结果与预测的现象不一致的是
| |
①中的物质 |
②中的物质 |
预测①的现象 |
| A |
淀粉KI溶液 |
浓硝酸 |
无明显变化 |
| B |
酚酞溶液 |
浓盐酸 |
无明显变化 |
| C |
AlCl3溶液 |
浓氨水 |
有白色沉淀 |
| D |
湿润红纸条 |
饱和氯水 |
红纸条褪色 |
下列离子方程式书写正确的是( )
| A.明矾溶液与氢氧化钡溶液反应,使SO恰好完全沉淀:Al3++2SO+2Ba2++3OH-===2BaSO4↓+Al(OH)3↓ |
| B.向FeBr2溶液中通入过量氯气:2Fe2++Cl2===2Fe3++2Cl- |
| C.用铂电极电解MgCl2溶液时发生的反应:2Cl-+2H2OCl2↑+H2↑+2OH- |
| D.常温下将硝酸铵溶液与KOH溶液混合:NH+OH-===NH3·H2O |
图中,Z为浸透饱和食盐水和酚酞试液的滤纸,水槽中盛有足量CuSO4溶液,X、Y为石墨电极。接通电路后,发现Z上的d点显红色。下列说法正确的是( )
| A.接通电路后,水槽中溶液的pH不变 |
| B.b是正极,Y电极上发生氧化反应 |
| C.同温同压下,X、Y两电极上产生气体的体积相等 |
| D.d点显红色是因为接通电路后OH-向d点移动 |
化学中常用图象直观地描述化学反应的进程或结果。下列图象描述正确的是( )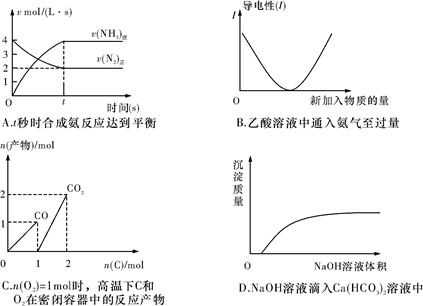
8gA和17gB混合,在某温度时汽化,气体体积为480mL,若在相同条件下汽化2gA和7gB的混合物,则汽化后的体积为160mL,则A、B可能为下列哪组物质( )
A.C2H4、C2H2 B.C2H4、CH3OH
C.C2H2、C6H6 D.CH2O、CH3COOH
下列事实不能用金属活动性解释的是( )
| A.镀锌铁制品破损后,镀层仍能保护铁制品 |
| B.工业上常用热还原法冶炼铁,用电解法冶炼钠 |
| C.电解法精炼铜时,其含有的Ag、Au杂质沉积在电解槽的底部 |
D. 生活中可用铝制的水壶烧水 生活中可用铝制的水壶烧水 |