某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度 (×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是___________。
A.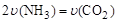 B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:__________________________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量______(填“增加”、“减小”或“不变”)。
④氨基甲酸铵分解反应的焓变△H____0,熵变△S___0(填>、<或=)。
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。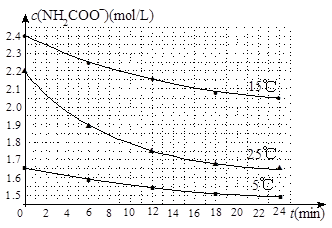
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率___________________________。
⑥根据图中信息,如何说明水解反应速率随温度升高而增大:_______________________。
向FeCl2和FeCl3混合溶液中加入适量KOH,高速搅拌下加入油脂,过滤后干燥得到一类特殊的磁流体材料,其化学式通式为KxFeO2(其组成可理解为aK2O·bFeO·cFe2O3)。请回答下列问题:
(1)若x的平均值为1.3,则磁流体中Fe2+和Fe3+的质量之比为。
(2)若x为1.4,请写出该磁流体在稀硫酸条件下与足量的KI溶液反应的化学方程式:
将该反应设计为原电池,负极电极反应为,当消耗1L 1.1mol/L KI溶液时,外电路通过电子数刚好为NA个,则该电池的化学能转化为电能的转化效率为。
(3)为测定该磁流体中Fe2+的含量,取化学式为K1.5FeO2的样品2g溶解在稀硫酸中并稀释到100ml,取出2mL加入10ml 0.005mol/L的KMnO4(在酸性条件下KMnO4被Fe2+还原为Mn2+),充分反应后再加入150ml 0.001mol/L的FeSO4,溶液紫红色恰好完全褪色,则原样品中Fe2+的质量分数为。溶解样品若选择稀硝酸测定结果(填偏高,偏低,无影响)
常见元素A、B、M组成的四种物质发生反应:甲+乙=丙+丁,其中甲由A和M组成,乙由B和M组成,丙只含有M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则乙的电子式为;生成标准状况下5.6L丙转移的电子数为;常温下丁溶液pH7,用离子方程式解释。
(2)若丁为能使品红褪色的无色气体,丙为常见红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。则①A在周期表中位置为②丁与水反应的化学方程式为向反应后溶液中滴加两滴紫色石蕊试液的现象为
③正确书写上述生成丙的化学方程式
④向MCl2的溶液中通入丁,可观察到白色的MCl沉淀,写出该反应的离子方程式。
甲、乙、丙、丁、戊五种短周期元素原子序数依次递增。甲最外层电子数是次外层的两倍,丙的次外层电子数比最外层少4个,丁形成的简单阳离子是同周期元素简单离子中半径最小的,戊是同周期主族元素中原子半径最小的。试用化学式回答下列问题:
(1)乙和戊形成的化合物中各原子最外层均满足8e-结构,其化学式为;
(2)写出乙的最高价氧化物的水化物的浓溶液与甲单质反应的化学方程式;
(3)戊的最高价氧化物与丁的最高价氧化物的水化物反应的离子反应方程式为;
(4)常温下戊单质被NaOH溶液吸收的化学方程式为;
(5)氢与丙形成原子个数比为1:1的液体,该物质中存在的作用力有()
①极性键②非极性键③离子键④氢键⑤范德华力
聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛用于制作光导纤维。已知A为某种聚甲基丙烯酸酯纤维的单体,其转化关系如下:
请回答下列问题:
(1)由B转化为C的反应类型为_____________,
(2)F含有的官能团名称为,简述检验该官能团的化学方法
(3)A的结构简式为______________________________________________________
(4)写出反应C→D的化学方程式:______________________________________。
(5)写出满足下列条件的B的链状同分异构体的结构简式:___________________________。
①能与NaOH溶液反应②能发生银镜反应
锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的核外电子排布式:。与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有(填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为。
(2)PO43-的空间构型是。
(3)与NH3互为等电子体的分子、离子有、(各举一例)。
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为。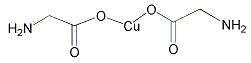
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1 mol CN-中含有的π键的数目为。
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为。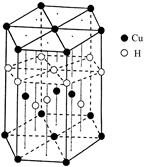
(7)铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,列式计算晶体铜的密度。