影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。
| 序号 |
条件 |
现象 |
结论 |
|
| 温度/℃ |
催化剂 |
|||
| 1 |
40 |
FeCl3溶液 |
|
|
| 2 |
20 |
FeCl3溶液 |
|
|
| 3 |
20 |
MnO2 |
|
|
| 4 |
20 |
无 |
|
|
试回答:
①实验1、2研究的是 对H2O2分解速率的影响。
②实验2、3的目的是 。
(2)实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
① 定性分析:如图甲可通过观察________________________________,定性比较得出结论。
有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________。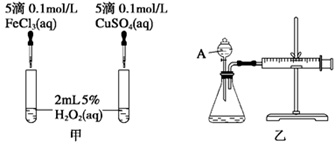
②定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是 。
(3)实验三:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是 。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
利用右图装置测定中和热的实验步骤如下:
①量取50mL 0.25mol•L-1硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol•L-1NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后,测量混合液温度。请回答:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________;
(2)NaOH溶液稍过量的原因_____________;
(3)加入NaOH溶液的正确操作是______(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是_______;
(5)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式 _____________;
| 温度 实验次数 |
起始温度t1/℃ |
终止温度 t2/℃ |
温度差平均值(t2-t1)/℃ |
||
| H2SO4 |
NaOH |
平均值 |
|||
| 1 |
25.0 |
25.2 |
25.1 |
28.5 |
|
| 2 |
24.9 |
25.1 |
25.0 |
28.3 |
|
| 3 |
25.5 |
26.5 |
26 |
31.8 |
|
| 4 |
25.6 |
25.4 |
25.5 |
29.0 |
(6)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) _______
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(7)______(填“能”或“不能”)用Ba(OH)2代替氢氧化钠溶液和稀硫酸反应;若将含0.5molH2SO4的 浓硫酸与含1molNaOH的溶液混合,放出的热量________(填“小于”、“等于”或“大于”)57.3kJ。原因是_______________________。
一学生设计了如下实验方法分离NaCl和CaCl2两种固体的混合物
填空和回答下列问题
(1)B物质是_______________(写化学式)
(2)按此实验方案分离得到的NaCl,经分析仍含有杂质,这是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是_______________
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是______________(填序号)
①混合物A②CaCl2固体③NaCl固体
某天然碱样品的组成可能为aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数),为确定其组成,某小组进行如下实验:
(1)定性实验:
①取少量样品放入试管中,用酒精灯加热,在试管口有液体生成,该液体能使无水硫酸铜变蓝,能否说明样品中是否含结晶水,简述理由_______________________。
②请设计一个简单方案,确认样品中含有CO32-_________________________。
(2)定量分析: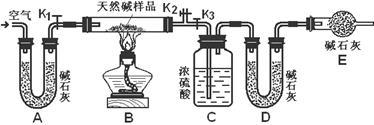
实验步骤:
①组装好实验装置后,首先进行的操作是______;A处碱石灰的作用是_________,E处碱石灰的作用是___________________________________。
②称7.3克样品,放入硬质玻璃管中,称量C装置质量为87.6克,D装置为74.7克。
③打开活塞k1、k2,关闭k3,通入空气数分钟。
④关闭k1、k2,打开k3,点燃酒精灯至不在产生气体为止。
⑤打开k1,鼓入空气数分钟,然后称得C装置质量为88.5克,D装置质量为75.8克,通入空气数分钟的目的是___________________________________。
⑥该天然碱的化学式为:_______________________________。
某研究性学习小组的同学利用下列装置进行乙醇催化氧化的实验。请分析回答:
(1)请写出实验过程中的总的化学反应方程式__________________________。
(2)在不断鼓入空气的情况下,移去酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是________反应。进一步研究表明,鼓气速度与反应体系的温度关系曲线如右图所示。鼓气速度过快,反应体系温度反而下降的原因___________________________。
(3)甲和乙两个水浴作用不相同。
甲的作用是________________;乙的作用是_________________________。
(4)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是___________。集气瓶中收集到的气体的主要成分是_______________。
(5)在检验生成物的过程中,一位同学很偶然地发现向溴水中加入乙醛溶液,溴水褪色。针对溴水褪色的原因,该小组的同学们经过分析后,提出两种猜想:
①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。
请你设计一个简单的实验,探究哪一种猜想正确?_______________________。
某化学课外活动小组欲制取纯碱Na2CO3溶液并讨论实验过程中的相关问题。可供选择的试剂有:A大理石;B盐酸;C氢氧化钠溶液;D澄清石灰水。
三名同学设计的制备方案的反应流程分别如下: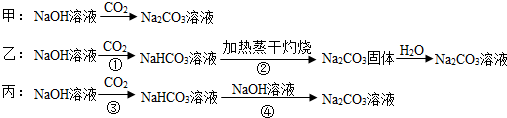
(1)请指出甲、乙两方案的主要缺点:
甲方案_______________________;
乙方案_______________________;
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键有______________________;
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3.乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学能否达到实验目的? ______________(填“能”或“不能”)若能,请说明其计算所需的数据;若不能,请简要说明理由______________。