已知氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1KJ,破坏1 mol氯气中的化学键消耗的能量为Q2KJ,形成1 mol氯化氢中的化学键释放的能量为Q3KJ,则下列关系式中一定正确的是( )
| A.Q1+Q2<2Q3 | B.Q1+Q2>2Q3 | C.Q1+Q2<Q3 | D.Q1+Q2=Q3 |
对照实验是研究物质性质的一种重要方法,下列不是用来做对照实验的是()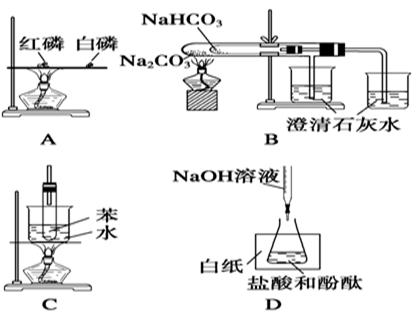
已知NH4CuSO3与足量的2mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是()
| A.反应中硫酸作氧化剂 | B.NH4CuSO3中硫元素被氧化 |
| C.1molNH4CuSO3完全反应转移0.5mol电子 | |
| D.刺激性气味的气体是氨气 |
25℃、101kPa下,反应2N2O5(g)=4NO2(g)+O2(g)△H=+56.7kJ/mol能自发进行的原()
| A.是吸热反应 | B.是放热反应 |
| C.是熵减小的反应 | D.熵增效应大于热效应 |
将氯水分别滴入下列各选项所述的溶液中,由实验现象得出的结论完全正确的是()
| 选项 |
氯水滴入下列溶液中 |
实验现象 |
结论 |
| A |
滴有KSCN的FeCl2溶液 |
变红 |
Cl2具有还原性 |
| B |
滴有酚酞的NaOH溶液 |
褪色 |
Cl2具有酸性 |
| C |
紫色石蕊溶液 |
先变红后褪色 |
Cl2具有漂白性 |
| D |
KI淀粉溶液 |
变蓝色 |
Cl2具有氧化性 |
下列5项内容中,排列顺序正确的有几项()
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②相同物质的量浓度的下列溶液中NH4+ 的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl
③微粒半径:K+>S2->F
④给出质子的能力:CH3COOH>C2H5OH>H2O
⑤氢化物的沸点:HI>HCl>HF
| A.1项 | B.2项 | C.3项 | D.4项 |