相同温度下,两个恒压且压强相同的密闭容器中发生可逆反应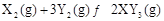

实验测得反应在起始及达到平衡时的有关数据如下表所示:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
0.1 |
0.3 |
0 |
4.63 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>O)kJ |
下列叙述正确的是( )
A.反应的平衡常数:①>②
B.达平衡时,两个容器中XY3的物质的量浓度均为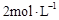
C.若容器①体积为0.20L.则达平衡时放出的热量大于4.63kJ
D.达到平衡时,容器①、②中各物质的百分含量相同
用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制0.2 mol·L-1的稀H2SO4
在配制过程中,下列操作中能引起误差偏高的有( )
| A.未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中 |
| B.转移前,容量瓶中含有少量蒸馏水 |
| C.定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线 |
| D.定容时,仰视刻度线 |
下列关于卤素的叙述中正确的是( )
① 加碘盐中,碘的存在形式为I2
② 溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯
③ 溴化银具有感光性,碘化银不具感光性
④ 检验Cl2气体中是否混有HCl可将气体通入硝酸银溶液
⑤氯气跟水反应时,水既不是氧化剂也不是还原剂
| A.①②⑤ | B.②④ | C.②⑤ | D.①③④ |
下列关于氯的说法正确的是( )
| A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂 |
| B.35 17Cl、37 17Cl为不同的核素,有不同的化学性质 |
| C.工业上,利用电解饱和食盐水获得Cl2 |
| D.1.12LCl2含有1.7NA个质子(NA表示阿伏伽德罗常数) |
下列说法正确的是( )
| A.液态HCl和固体NaCl均不导电,所以HCl、NaCl均是非电解质 |
| B.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质 |
| C.铜、石墨均导电,但他们都不是电解质,而是非电解质 |
| D.蔗糖、酒精在水溶液或熔融状态下均不导电, 所以它们均是非电解质 |
下列物质中既能跟氢氧化钠溶液反应, 又能跟稀HCl反应的是( )
①Al2O3 ②Al(OH)3③(NH4)2CO3 ④NaHCO3 ⑤BaCl2
| A.③④⑤ | B.②③④⑤ | C.①②③④ | D.全部 |