下列溶液中Cl-浓度与50 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是
| A.150 mL 1 mol·L-1的NaCl溶液 |
| B.75 mL 2 mol·L-1 NH4Cl溶液 |
| C.25 mL 1.5 mol·L-1的MgCl2溶液 |
| D.25 mL 2 mol·L-1的FeCl3溶液 |
在某温度时,测得纯水中的c(H+)=2.4×10-7 mol/L,则c(OH-)为( )
| A.2.4×10-7 mol/L | B.1.0×10-7 mol/L |
C.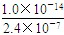 mol/L mol/L |
D.c(OH-)无法确定 |
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)=CO2(g)ΔH1 C(s)+1/2O2(g)=CO(g)ΔH2
②S(s)+O2(g)=SO2(g)ΔH3 S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+1/2O2(g)=H2O(l)ΔH5 2H2(g)+O2(g)=2H2O(l)ΔH6
④CaCO3(s)=CaO(s)+CO2(g)ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s)ΔH8
| A.① | B.④ | C.②③④ | D.①②③ |
自然界的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用。例如桂皮中的肉桂醛就是其中的一种,已知肉桂醛的结构简式为:  ,下列关于肉桂醛的说法中不正确的是( )
,下列关于肉桂醛的说法中不正确的是( )
| A.该化合物的分子式为C9H8O |
| B.能发生银镜反应 |
| C.既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
| D.1mol该有机物最多只能与2mol氢气发生加成反应 |
将PH试纸湿润后测量以下溶液,不会产生误差的是( )
| A.Na2SO4 | B.Al2(SO4)3 | C.HNO3 | D.KOH |
为了除去FeCl2溶液中混有的少量FeCl3,最好的方法是向此溶液中( )
| A.通入氯气 | B.加入NaOH | C.加入Fe | D.加入Cu |