某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示: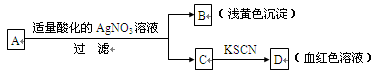
现对A、B、C、D作出的如下推断中,不正确的是
A.盐A一定是FeBr3 B.浅黄色沉淀B是AgBr
C.滤液C中一定含Fe3+ D.D溶液中有Fe(SCN)3
下表中关于离子方程式评价合理的是
| 选项 |
化学反应及其离子方程式 |
评价 |
| A |
醋酸钠溶于水:CH3COO-+H2O===" " CH3COOH+OH- |
正确 |
| B |
在氢氧化钠溶液中滴加少量氯化铝: Al3++3OH-===Al(OH)3↓ |
错误,Al(OH)3能溶于氢氧化钠 |
| C |
铁加入到过量的稀硝酸溶液中:3Fe + 8H++2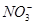 ===3Fe2++ 2NO↑ + 4H2O ===3Fe2++ 2NO↑ + 4H2O |
正确 |
| D |
在硫酸铝钾溶液中滴加氢氧化钡溶液至沉淀的物质的量最多:3Ba2++6OH-+2Al3++3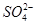 === 3BaSO4↓+2Al(OH)3↓ === 3BaSO4↓+2Al(OH)3↓ |
错误,Al3+与OH-的化学计量数之比为1∶3 |
室温时,下列各组离子在指定溶液中可以大量共存的是
A.由水电离出的c(H+)=10-12mol/L的溶液中:Na+、Ba2+、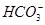 、Cl- 、Cl- |
| B.无色透明溶液中:K+、Cu2+、SO42-、Na+ |
C.含有大量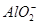 的溶液中:Na+、OH-、Cl-、 的溶液中:Na+、OH-、Cl-、 |
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、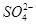 |
有关电解质溶液的叙述,下列说法中正确的是
A.0.2 mol·L-1氨水中,c(OH-)与c(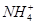 )相等 )相等 |
| B.10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
| C.0.1 mol/L的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D.pH=3的一元酸和pH=11的一元碱等体积混和后的溶液中一定是c(OH-)=c(H+) |
a、b、c、d、e五种短周期主族元素,在元素周期表中的相对位置如下表。b与d可以形成两种常见的化合物,下列说法错误的是
| a |
b |
|||
| c |
d |
e |
A.元素c的氧化物具有两性
B.原子半径的大小顺序为:a>b>c>d>e
C.b元素在地壳中的含量居第一位
D.元素d的非金属性小于e
下列说法不正确的是
| A.2013年0点钟声敲响后的几个小时,北京的污染指数从轻度污染上升为重度污染,主要污染为PM2.5污染,看来烟花爆竹的燃放,可加重PM2.5污染 |
| B.催化剂之所以能加快反应速率,是因为催化剂能降低反应的活化能 |
| C.氨气的水溶液氨水可以导电,因此氨气是电解质 |
| D.大量燃烧含硫燃料是形成酸雨的主要原因 |