反应4A(s)+3B(g) 2C(g)+ D(g),经2min,B的浓度减少0.6mol/L。对此反应速率的表示正确的是( )
2C(g)+ D(g),经2min,B的浓度减少0.6mol/L。对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示的反应速率其比值是3:2:1
C.在2min末的反应速率,用B表示是0.3 mol·(L·min)-1
D.在这2min内用B和C表示的反应速率的值都是逐渐减小的
常温下,有下列四种溶液:
| ① |
② |
③ |
④ |
| 0.1mol/L NH3·H2O溶液 |
pH=11 NaOH溶液 |
pH=1 H2SO4溶液 |
pH=3 CH3COOH溶液 |
下列说法正确的是()
A.①与③等体积混合,溶液pH<7
B.②与④等体积混合,溶液pH>7
C.将VmL④的溶液浓缩到10—2VmL后,pH与③相同
D.②与③混合,若溶液pH=7,则V(NaOH) : V(H2SO4) =100 : 1
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
| A.放电时负极附近溶液的pH不变 |
| B.放电时电解质溶液中的OH-向正极移动 |
| C.充电时电池的负极应与电源的负极相连接 |
| D.充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
在容积可变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g) ΔH<0,某研究小组研究了其他条件不变时,只改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g) ΔH<0,某研究小组研究了其他条件不变时,只改变某一条件对上述反应的影响,下列分析正确的是( )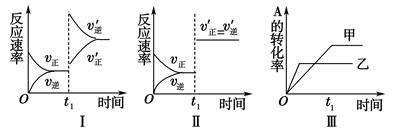
| A.图Ⅰ表示的是t1时刻升高温度对反应速率的影响 |
| B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高 |
| D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高 |
一定条件下,对于可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.12 mol/L,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.12 mol/L,则下列判断正确的是( )
| A.c1 : c2=1 : 3 |
| B.平衡时,3VY (正) =2VZ (逆) |
| C.X、Y的转化率相等 |
| D.c1的取值范围为0.06<c1<0.16 mol/L |
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g)△H=Q kJ·mol-1;反应达到平衡时,X的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g)△H=Q kJ·mol-1;反应达到平衡时,X的物质的量浓度与温度、气体体积的关系如下表所示:
| 容器体积/L c(X)/mol·L—1 温度/℃ |
1 |
2 |
3 |
| 100 |
1.00 |
0.75 |
0.53 |
| 200 |
1.20 |
0. 90 |
0.63 |
| 300 |
1.30 |
1.00 |
0.70 |
下列说法正确的是( )
A.m>n
B.温度不变,增大体积,X的转化率增大
C.Q<0
D.体积不变,温度升高,平衡向正反应方向移动