相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:
2SO2(g)+O2(g)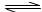 2SO3(g);
2SO3(g);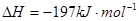 。实验测得起始、平衡时的有关数据如下表:
。实验测得起始、平衡时的有关数据如下表:
| 容器 |
起始各物质的物质的量/mol |
达到平衡时体系能量的变化 |
|||
| SO2 |
O2 |
SO3 |
Ar |
||
| 甲 |
2 |
1 |
0 |
0 |
放出热量:Q1 |
| 乙 |
1.8 |
0.9 |
0.2 |
0 |
放出热量:Q2 |
| 丙 |
1.8 |
0.9 |
0.2 |
0.1 |
放出热量:Q3 |
下列叙述正确的是
A.Q1=Q2=Q3="197" kJ
B.达到平衡时,丙容器中SO2的体积分数最大
C.甲、乙、丙3个容器中反应的平衡常数相等
D.若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1<-197 kJ·mol-1
某核素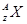 可形成HmX型氢化物,则 a g HmX 含有()
可形成HmX型氢化物,则 a g HmX 含有()
A.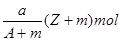 质子 质子 |
B. 电子 电子 |
C. 中子 中子 |
D.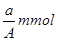 |
下列除杂试剂的选择或除杂操作不正确的是
| 括号内为杂质 |
除杂试剂 |
除杂操作 |
|
| A |
Na2O2(Na2O)固体 |
O2 |
在纯氧气中加热 |
| B |
Na2CO3 (NaHCO3)溶液 |
CO2 |
通入过量的 CO2 |
| C |
FeCl3(FeCl2)溶液 |
Cl2 |
通入过量的 Cl2 |
| D |
FeSO4(CuSO4)溶液 |
Fe |
加入过量的 Fe 粉,充分反应后过滤 |
烧杯中盛有一定量的液态物质A,加入少量固体物质B,B不溶解。当通入气体C时发现B逐渐溶解直至完全溶解。则 A、B、C依次为()
A.H2O、BaSO4、O2 B.FeCl2溶液、Fe粉、Cl2
C.H2O、CaCO3、SO3气体 D.H2O、SiO2、HCl气体
甲、乙、丙三种物质之间能通过一步反应实现转化关系: 甲 乙
乙 丙,则甲、丙不可能是
丙,则甲、丙不可能是
| A.NO HNO3 | B.CH2=CH2CH3CHO | C.Fe FeCl3 | D.Si H2SiO3 |
在容积固定的密闭容器中存在如下反应:N2(g)+3H2(g)  2NH3(g) ΔH<0。 某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如下关系图。下列叙述正确的是()
2NH3(g) ΔH<0。 某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如下关系图。下列叙述正确的是()
| A.图Ⅰ研究的是温度对反应的影响,且甲的温度比乙的高 |
| B.图Ⅱ研究的是温度对反应的影响,且甲的温度比乙的高 |
| C.图Ⅱ研究的是压强对反应的影响,且甲的压强比乙的大 |
| D.图Ⅲ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率比甲使用的高 |