含苯酚的工业废水处理的流程图如下: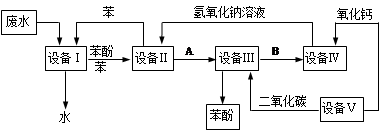
(1) 上述流程里,设备Ⅰ中进行的是_______________操作(填写操作名称)。
(2) 由设备Ⅱ进入设备Ⅲ的物质A是________。由设备Ⅲ进入设备Ⅳ的物质B是________。
(3) 在设备Ⅲ中发生反应的化学方程式为_________________________________________。
(4) 在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和_________,通过操作_________ (填写操作名称)可以使产物相互分离。
(5) 上图中能循环使用的物质是C6H6、CaO、___________、___________。
氯化钠溶液在生产、生活中都有广泛的用途。现配置1 L 0.2 mol·L-1NaCl溶液,请回答问题。
| 实验步骤 |
有关问题 |
| (1)计算并称量 |
用托盘天平称量NaCl固体的质量为g |
| (2)溶解 |
为加速溶解,可进行的操作是 |
(3)转移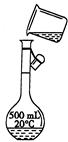 |
指出示意图中的两处错误: 错误1: 错误2: |
| (4)洗涤 |
用少量蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中 |
| (5)定容 |
若俯视容量瓶刻度线,定容后会造成所配溶液的物质的量浓度(填“偏高”“偏低”或“无影响”) |
有机物分子式的确定常采用燃烧法,其操作如下:在电炉加热下用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。如图所示是用燃烧法测定有机物分子式常用的装置,其中A管装碱石灰,B管装无水CaCl2。现准确称取1.80 g有机物样品(含C、H元素,还可能含有O元素),经燃烧被吸收后A管质量增加1.76 g,B管质量增加0.36 g。请按要求填空:
(1)此法适宜于测定固体有机物的分子式,此有机物的组成元素可能是________。
(2)产生的气体按从左到右的流向,所选各装置导管口的连接顺序是________。
(3)E和D中应分别装有何种药品________。
(4)如果将CuO网去掉,A管增加的质量将________(填“增大”“减小”或“不变”)。
(5)该有机物的最简式是________________。
(6)要确定该有机物的分子式,还必须知道的数据是________。
A.消耗液体E的质量 B.样品的摩尔质量
C.CuO固化减少的质量 D.C装置增加的质量
E.燃烧消耗氧气的物质的量
(7)在整个实验开始之前,需先让D产生的气体通过整套装置一段时间,其目的是_________________________________________________________________。
为测定某品牌洗厕精的酸(盐酸)含量,某学生欲用已知物质的量浓度的NaOH溶液来测定该洗厕精(盐酸)的物质的量浓度时,选择酚酞作指示剂。请填写下列空白:
(1)碱式滴定管的使用方法,正确步骤的先后顺序为(填选项符号):
A.用氢氧化钠溶液润洗仪器并加入氢氧化钠溶液
B.放出氢氧化钠溶液进行滴定
C.调节起始读数
D.查漏,再水洗2-3遍
(2)用标准的NaOH溶液滴定待测的盐酸时,左手控制碱式滴定管的玻璃球,右手摇动锥形瓶,眼睛应注视;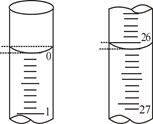
(3)若滴定开始和结束时,碱式滴定管中的液面如上图所示:则所用NaOH溶液的体积为mL。
(4)某学生根据三次实验分别记录有关数据如下表:
| 滴定次数 |
待测盐酸的体积/mL |
0.1000 mol/LNaOH溶液的体积/mL |
||
| 滴定前刻度 |
滴定后刻度 |
溶液体积/mL |
||
| 第一次 |
25.00 |
2.00 |
28.15 |
26.15 |
| 第二次 |
25.00 |
1.50 |
29.50 |
28.00 |
| 第三次 |
25.00 |
0.20 |
26.55 |
26.35 |
请选用其中合理的数据计算该洗厕精中酸(盐酸)的物质的量浓度:
c(HCl)=。
(5)分析下列操作对所测洗厕精的酸(盐酸)的浓度的影响:(填“偏大”、“偏小” 或“无影响”)
A.若取待测液时,开始仰视读数, 后俯视读数,则;
B.若碱式滴定管在滴定前有气泡,滴定后气泡消失,则。
TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元素组成,与氢气的相对分子质量之比为120。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。其主要过程为在足量氧气流中将4.80 g TMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热装置等已略去,其他用品可自选)。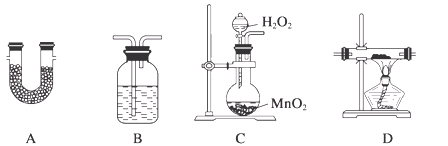
(1)将所选用的仪器(可重复选用)连接顺序由上到下依次填入下表,并写出该仪器中应加入的试剂的名称及作用。
| 选用的仪器 |
加入试剂 |
加入试剂的作用 |
| C |
H2O2溶液与MnO2 |
产生氧气 |
| D |
CuO粉末 |
将可能生成的CO转化为CO2 |
(2)实验后称得A及以后的装置(均用A装置并假设每次吸收均是完全的)质量依次增加3.60 g、14.08 g、0.14 g,则TMB的分子式为__________________________。
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下: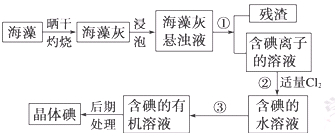
(1)指出操作③的名称:;操作②中充入适量Cl2的目的是。
(2)提取碘的过程中,可供选择的试剂是 ( )
| A.酒精 | B.四氯化碳 | C.汽油 | D.醋酸 |
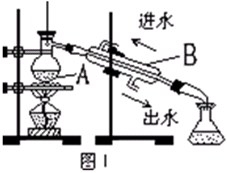
(3)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏。图I是某同学设计的蒸馏装置,图中明显的错误是。
(4)有同学认为蒸馏时最好使用水浴加热,使用水浴的优点是:;蒸馏结束,晶体碘聚集在(填仪器名称)里。
(5) 实验③分离出来的废液中含有Cl–、SO42–,现只取一次试液,如何鉴别出Cl–、SO42–,依次加入试剂的为:、。
(6)某小组同学实验时需用到一定物质的量浓度的碘水溶液225mL,配制时需要的仪器除天平、玻璃棒、烧杯外,还需、。若摇匀时,发现液面低于刻度线,则配得溶液浓度(填偏大、偏小或无影响)。