某溶液中加入氯化钡溶液生成白色沉淀,再加入稀硝酸沉淀不溶解,这溶液中
| A.一定含有SO42— | B.一定含有Ag+ |
| C.可能含有SO42—或Ag+ | D.可能含有CO32— |
最近医学界通过用放射性15C跟踪标记C60, 发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),则有关15C的叙述正确的是
| A.与C60中普通碳原子的化学性质不同 | B.与16O的中子数相同 |
| C.是金刚石的同素异形体 | D.与12C互为同位素 |
下图是一种航天器能量储存系统原理示意图。下列说法正确的是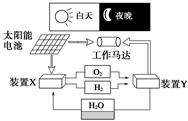
| A.该系统中只存在3种形式的能量转化 |
| B.装置Y中负极的电极反应式为O2+2H2O+4e-===4OH- |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
Cd + 2NiOOH + 2H2O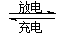 Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.放电时正极反应:NiOOH + H2O- e— ="=" Ni(OH)2 + OH-
B.充电过程是化学能转化为电能的过程
C放电时Cd是负极,发生氧化反应
D.放电时电解质溶液中的OH-向正极移动
下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是(ΔH用于表示反应中的热量变化,ΔH>0表示反应吸热 ,ΔH<0 表示反应放热)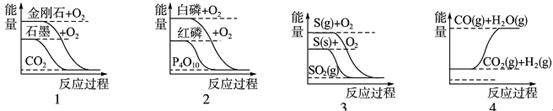
| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)===SO2(g) ΔH2则ΔH1>ΔH2 |
| D.CO(g)+H2O(g)===CO2(g)+H2(g) ΔH1>0 |
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活动性相差越大,电压表的读数越大)依据记录数据判断,下列结论中正确的是
| 金属 |
电子流动方向 |
电压/V |
| 甲 |
甲→Cu |
0.78 |
| 乙 |
Cu→乙 |
0.15 |
| 丙 |
丙→Cu |
1.35 |
| 丁 |
丁→Cu |
0.30 |
A.金属乙能从硫酸铜溶液中置换出铜
B.甲、乙形成合金时,将该合金露置在空气中,甲先被腐蚀
C.在四种金属中,乙的还原性最强
D.甲、丁若形成原电池时,甲为正极