已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
用图中所示的装置进行实验,实验现象与预测不一致的是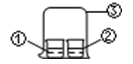
| ①中的物质 |
②中的物质 |
预测现象 |
|
| A |
浓氨水 |
FeCl3溶液 |
②中有红褐色沉淀 |
| B |
浓氨水 |
浓盐酸 |
③中有白烟 |
| C |
浓硝酸 |
淀粉KI溶液 |
②中溶液为蓝色 |
| D |
饱和亚硫酸溶液 |
蓝色石蕊试液 |
②中溶液先变红又褪色 |
化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中,属干这种情况的是
①过量锌与18 mol/L的硫酸反应;
②过量氢气与少量氮气在催化剂存在下充分反应;
③浓盐酸与过量的MnO2反应;
④过量铜与浓硫酸反应;
⑤过量稀硝酸与银反应;
⑥过量稀硫酸与大块状石灰石反应。
| A.②③④⑥ | B.②③⑤ | C.①④⑤ | D.①②③④⑤⑥ |
某有机化合物的结构简式为: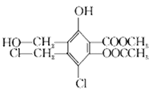 ,下列有关该物质的叙述正确的是
,下列有关该物质的叙述正确的是
| A.1 mol该物质最多可以消耗3 mol Na |
| B.1 mol该物质最多可以消耗7 mol NaOH |
| C.不能与Na2CO3溶液反应 |
| D.易溶于水,可以发生加成反应和取代反应 |
下列各组物质,不能按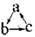 (“→”表示反应一步完成)关系转化的是
(“→”表示反应一步完成)关系转化的是
| 选项 |
a |
b |
c |
| A |
Al2O3 |
NaAlO2 |
Al(OH)3 |
| B |
AlCl3 |
Al(OH)3 |
NaAlO2 |
| C |
Al |
Al(OH)3 |
Al2O3 |
| D |
MgCl2 |
Mg(OH)2 |
MgO |
为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是
①Na2O2中阴、阳离子的个数比是1:1
②Na2O2分别与水及CO2反应产生等量氧气时,需水和CO2的质量相等
③Na2O2分别与水及CO2反应产等量氧气时,转移电子的物质的量相等
④Na2O2的漂白原理与SO2的漂白原理相同
⑤Na2O2与SO2反应生成Na2SO3与H2O
⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
⑦Na2O2与水反应,Na2O2既是氧化剂,又是还原剂
⑧Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色
| A.①③⑥⑧ | B.③⑦⑧ | C.②⑤⑥⑦ | D.①④⑧ |